Die Kenntnisse über die Reaktionsmechanismen sind in der organischen Chemie notwendig, um chemische Verbindungen herstellen zu können. Wenn ein Molekül oder ein Ion Elektronen aufnehmen kann, bezeichnet man es als elektrophil („elektronenliebend“). Kann ein Molekül oder Ion Elektronen zur Verfügung stellen, so ist es nukleophil (ursprünglich „kernliebend“, heute in der Bedeutung „elektronenspendend“). Der „Angriff“ auf ein stabiles Molekül erfolgt mit einem anderen Teilchen, das fähig ist, das Molekül zu aktivieren. Chemische Reaktionen in der organischen Chemie beruhen auf Veränderungen der Elektronenverteilung und der Elektronenpaarung.
Nukleophile sind Moleküle oder Ionen, die Elektronen zur Verfügung stellen und diese zur Bildung einer neuen Bindung einsetzen können. Typische Nukleophile sind zum Beispiel:
Br− CN− H2O (schwach) C=C-Doppelbindungen Basen wie NH3 oder OH−
Elektrophile sind Moleküle oder Ionen, die Elektronen aufnehmen können. Elektrophile ziehen Elektronen an und nehmen sie zur Bindungsbildung auf. Typische Elektrophile sind zum Beispiel:
Brδ+ (positiv polarisiertes Brom-Atom) NO2+ (Nitronium-Ion) H+ (Proton einer Säure)
Radikale sind Moleküle oder Atome, die mindestens ein ungepaartes Elektron besitzen. Sie sind sehr reaktionsfreudig, da sie bestrebt sind, wieder einen stabileren Zustand mit gepaarten Elektronen zu erreichen. Radikale entstehen typischerweise durch Spaltung einer Bindung, zum Beispiel durch hohe Temperatur oder UV-Licht, wobei jeder Bindungspartner ein Elektron erhält. Sauerstoff-, Chlor- oder Brom-Moleküle liefern gerne Radikale, Peroxide ebenfalls. Beispiele:
Br2 → Br· + ·Br H2O2 → HO· + ·OH
Radikale besitzen weder einen Elektronenüberschuss noch einen Elektronenmangel im klassischen Sinn. Sie sind daher weder nukleophil noch elektrophil, sondern reagieren, um ihr ungepaartes Elektron zu paaren. Radikale reagieren häufig mit σ-Bindungen (zum Beispiel C–H-Bindungen) oder mit π-Bindungen (zum Beispiel C=C-Doppelbindungen), indem sie neue Bindungen ausbilden.
Schwachstellen in organischen Molekülen
Wie kann man Schwachstellen in Molekülen erkennen? Die Schwachstellen sind Atome oder Bindungen, an denen chemische Reaktionen bevorzugt ablaufen. Ursache sind stets Ungleichverteilungen von Elektronendichte oder instabile Bindungssituationen. Im Folgenden werden die wichtigsten Arten solcher Schwachstellen erläutert.
1. Polare Bindungen, freie Elektronenpaare. In einer polaren Bindung sind die Bindungselektronen ungleich verteilt. Das elektronegativere Atom zieht die Elektronen stärker an und trägt eine partielle negative Ladung (δ−), das andere Atom trägt eine partielle positive Ladung (δ+). Atome mit partieller positiver Ladung sind bevorzugte Angriffspunkte, da sie elektronenarm sind. Typische Beispiele für polare Bindungen sind:
C–O C–N C–Cl C–Br O–H N–H
Chemisch gebundene Sauerstoff-, Stickstoff- oder Halogen-Atome besitzen in vielen organischen Verbindungen freie Elektronenpaare. Diese Elektronen sind nicht an der Bindung beteiligt, sie stehen für die Bildung neuer Bindungen zur Verfügung.
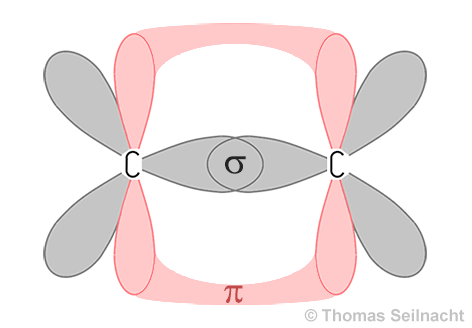
2. Mehrfachbindungen. Doppel- und Dreifachbindungen bestehen aus verschiedenen Bindungsarten. Neben einer σ-Bindung (Sigma-Bindung) enthalten sie gemäß dem Hybridorbitalmodell eine oder zwei π-Bindungen (Pi-Bindungen). Beispiele:
C–C (Alkane): eine σ-Bindung
C=C (Alkene): eine σ-Bindung und eine π-Bindung
C≡C (Alkine): eine σ-Bindung und zwei π-Bindungen
C=O (Carbonylgruppe): eine σ-Bindung und eine π-Bindung
π-Bindungen sind im Vergleich zu σ-Bindungen reaktionsfreudiger. Die π-Elektronen wirken nukleophil. Besonders reaktiv ist die C=O-Doppelbindung der Carbonylgruppe, da sie zusätzlich eine starke Polarität aufweist. Das Kohlenstoff-Atom der Carbonylgruppe ist elektrophil. Dadurch kann es durch Nukleophile wie CN− angegriffen werden.
3. Stabilität der entstehenden Moleküle oder Ionen. Bindungen lassen sich besonders leicht lösen, wenn bei der chemischen Reaktion stabile Ionen oder Moleküle entstehen. Dies ist eine wichtige Voraussetzung für Substitutions- und Eliminierungsreaktionen. Typische Beispiele:
- Ist in einem organischen Molekül ein Halogen-Atom (zum Beispiel Cl, Br oder I) an ein Kohlenstoff-Atom gebunden, so kann sich diese Bindung lösen, wobei das Halogen-Atom die Bindungselektronen vollständig mitnimmt. Dabei entsteht ein Halogenid-Ion, das relativ stabil ist. Deshalb lassen sich solche Bindungen vergleichsweise leicht spalten.
- Bei Alkoholen ist die C-O-Bindung zwischen dem Kohlenstoff-Atom und dem Sauerstoff-Atom zunächst schwer zu spalten. Nimmt das Sauerstoff-Atom jedoch ein Proton (H+) auf, spricht man von Protonierung. Diese führt zum Lösen der Bindung, das Molekül wird dann umgebaut, zum Schluss spaltet sich ein Wasser-Molekül (H2O) ab. Das Proton selbst wird dabei nicht verbraucht, es wirkt katalytisch.
- Benzol reagiert mit Brom, wenn ein Katalysator wie FeBr3 vorhanden ist. Es entsteht zunächst eine instabile, positiv geladene Zwischenverbindung, die nicht aromatisch und daher energetisch ungünstig ist. Durch die Abspaltung eines Protons wird die Aromatizität am Benzolring wiederhergestellt. Das entstehende Brombenzol ist deutlich stabiler als die Zwischenverbindung.
Beispiele für die verschiedenen Reaktionstypen in der organischen Chemie
Die Benennung des Reaktionstyps erfolgt zuerst nach dem Teilchen, das den Mechanismus der jeweiligen Reaktion charakterisiert (Elektrophil, Nukleophil, Radikal). Dann folgt die Art der Bindungsänderung (Addition, Substitution, Eliminierung). Bei der Symbolschreibweise wird zuerst die Bindungsänderung genannt, dann folgt das Symbol für den Mechanismus. In deutschen Schulbüchern ist dieses Symbol oft tiefgestellt.
| Reaktionstyp | Typischer Angriffsort | Reaktionsprinzip | Beispiele |
|---|---|---|---|
| Elektrophile Addition AE Mechanismus Folie |
π-Elektronen der C=C- bzw. C≡C-Bindung zwischen zwei C-Atomen | Die elektronenreiche Mehrfachbindung wirkt nukleophil. Sie polarisiert das Molekül des Reaktionspartners, dadurch wird ein Teil des Moleküls elektrophil und kann angreifen. Der andere Teil des Moleküls wird dann ebenfalls addiert. | Ethen reagiert mit Brom zu 1,2-Dibromethan. CH2=CH2 + Br2 → Br–CH2–CH2–Br |
| Nukleophile Addition AN |
Carbonyl-Kohlenstoff-Atom (Cδ+) der C=O-Gruppe | Ein Nukleophil (z.B. CN−), greift das elektrophile Kohlenstoff-Atom der Carbonylgruppe an. Dabei wird die Doppelbindung aufgelöst und das Nukleophil an das C-Atom gebunden. | Methanal reagiert mit Blausäure zu einem Hydroxynitril. HCHO + HCN → HO–CH2–CN |
| Radikalische Addition AR |
C=C-Doppelbindung zwischen zwei sp²-hybridisierten C-Atomen | Durch Bildung von Radikalen wird die Reaktion ausgelöst. Radikale greifen die Doppelbindung an und ermöglichen die Addition der Reaktionspartner. | Propen reagiert mit Bromwasserstoff zu 1-Brompropan, wenn Peroxid vorhanden ist. CH3–CH=CH2+HBr → CH3–CH2–CH2Br |
| Elektrophile aromatische Substitution SEAr Mechanismus Folie |
π-Elektronensystem des aromatischen Rings (C-Atome des Benzolrings) | Ein Elektrophil greift den aromatischen Ring an. Nach kurzzeitigem Verlust der Aromatizität wird diese wiederhergestellt. | Benzol reagiert mit Brom und FeBr3-Katalysator zu Brombenzol und Bromwasserstoff. C6H6 + Br2 → C6H5Br + HBr |
| Nukleophile Substitution SN1 Mechanismus Folie |
Tertiäres C-Atom nach Abgang eines Substituenten | Zuerst Abgang eines Substituenten vom tertiären C-Atom, dann Bindung des angreifenden Nukleophils am positiv polarisierten C-Atom. | tert-Butylchlorid reagiert mit Wasser zu tert-Butanol und Chlorwasserstoff. (CH3)3CCl+H2O → (CH3)3COH + HCl |
| Nukleophile Substitution SN2 Mechanismus Folie |
C-Atom, das mit einem negativ polarisierten Substituenten verbunden ist und dadurch positiv polarisiert wird | Gleichzeitiger Abgang eines Substituenten und Bindung des angreifenden Nukleophils am positiv polarisierten C-Atom. |
Iodmethan reagiert mit Hydroxid-Ionen zu Methanol und Iodid-Ionen. CH3I + OH− → CH3OH + I− |
| Radikalische Substitution SR Mechanismus Folie |
C–H-Bindung eines Alkans | Radikale ermöglichen den Austausch von Wasserstoff-Atomen durch andere Atome. Dabei können weitere Radikale entstehen. | Methan reagiert mit Chlor bei UV-Licht zu Chlormethan und Chlorwasserstoff. CH4 + Cl2 → CH3Cl + HCl |
| Eliminierung E1 |
H-Atome, die an C-Atomen sitzen, die mit einem tertiären C-Atom (nach Abgang eines Molekülteils) verbunden sind | Zuerst Abgang eines Molekülteils vom tertiären C-Atom, dann Entfernung eines H-Atoms von einem benachbarten C-Atom und Bildung einer Doppelbindung | tert-Butanol reagiert (säurekatalysiert) zu Isobuten und Wasser. (CH3)3C–OH → (CH3)2C=CH2 + H2O |
| Eliminierung E2 |
H-Atom an einem C-Atom, das mit einem benachbarten C-Atom verbunden ist, von dem sich ein Molekülteil löst. | Gleichzeitiger Abgang eines Molekülteils und eines H-Atoms von einem benachbarten C-Atom unter Bildung einer Doppelbindung. | Ethanol reagiert (säurekatalysiert) zu Ethen und Wasser. CH3–CH2OH → CH2=CH2 + H2O |
Bei den Reaktionen SN1 und E1 geht vor der eigentlichen Substitution oder Eliminierung zuerst ein Molekülteil weg. Erst dann ist das verbleibende Molekül so aktiviert, dass die Reaktion stattfinden kann. Bei den Reaktionen SN2 und E2 startet die Reaktion sofort.
Die bekannte Reaktion von 1,2-Dibromethan mit Zink ist eine Eliminierungsreaktion im allgemeinen Sinn, bei der in einer Reduktiven Dehalogenierung zwei Halogen-Atome von benachbarten C-Atomen entfernt werden und Ethen und Zinkbromid entstehen. Sie stellt keinen speziellen Eliminierungsmechanismus dar und lässt sich weder dem E1- noch dem E2-Mechanismus zuordnen.
Die säurekatalylsierte Esterreaktion zählt zu den Kondensationsreaktionen, es verbinden sich zwei Moleküle unter Abspaltung eines Wasser-Moleküls. Der eigentliche Angriff erfolgt nach der Protonierung der Carbonylgruppe durch die nukleophile OH-Gruppe des Alkohols.
Mechanismus des Esterreaktion Folie zur Esterreaktion
Die bekannte Reaktion von 1,2-Dibromethan mit Zink ist eine Eliminierungsreaktion im allgemeinen Sinn, bei der in einer Reduktiven Dehalogenierung zwei Halogen-Atome von benachbarten C-Atomen entfernt werden und Ethen und Zinkbromid entstehen. Sie stellt keinen speziellen Eliminierungsmechanismus dar und lässt sich weder dem E1- noch dem E2-Mechanismus zuordnen.
Die säurekatalylsierte Esterreaktion zählt zu den Kondensationsreaktionen, es verbinden sich zwei Moleküle unter Abspaltung eines Wasser-Moleküls. Der eigentliche Angriff erfolgt nach der Protonierung der Carbonylgruppe durch die nukleophile OH-Gruppe des Alkohols.
Mechanismus des Esterreaktion Folie zur Esterreaktion
Weitere Beispiele und Erklärungen in Kurzform
Additionen
Bei einer Addition kommen Atome oder Atomgruppen in ein bestehendes Molekül hinzu. Besonders aufnahmefähig sind ungesättigte Zweifach- oder Dreifachbindungen.
R–X + Y
- Brom reagiert mit Ethen zu einem Halogenalkan (Elektrophile Addition AE)
- Brom reagiert mit ungesättigten Fettsäuren (AE)
- Addition von Chlor an Ethin (AE mehrstufig)
- Bromwasserstoff reagiert mit Propen zu 1-Brompropan (mit Peroxiden: Radikalische Addition AR)
Substitutionen
Bei einer Substitution werden Atome oder Atomgruppen ausgetauscht (von engl. substitute, ersetzen).
R–X + Y
- Hexan reagiert mit Brom zu Bromhexan und Bromwasserstoff (Radikalische Substitution SR)
- Methanol reagiert mit HBr zu Brommethan und Wasser (Nukleophile Substitution SN)
- Iodmethan reagiert mit Natriumhydroxid zu Methanol und Natriumiodid (SN)
- tert-Butanol reagiert mit Bromwasserstoff zu tert-Butylchlorid und Wasser (SN)
- Benzol reagiert mit Brom zu Brombenzol und Bromwasserstoff (SEAr)
- Nitrierung von Phenol mit Salpetersäure zu Nitrophenol (SEAr)
- Sulfonierung eines Alkylbenzols (SEAr)
Eliminierungen
Bei einer Eliminierung wird ein Molekül M1 so verändert, dass zwei Atome oder Atomgruppen entfernt werden und dadurch ein weiteres Molekül M2 entsteht. Häufig bildet sich im veränderten Molekül M1' eine C=C-Doppelbindung.
M1
- Eliminierung von Wasser aus Ethanol mit Schwefelsäure (E2)
- Eliminierung von Brom aus 1,2-Dibromethan mit Zink (Dehalogenisierung)
Umlagerungen
Ein Substituent in einem Molekül löst sich und bildet eine neue Verknüpfung.
R–XY
Kondensationsreaktionen
Bei einer Kondensation verbinden sich zwei Moleküle unter Abspaltung eines kleinen Moleküls (meist Wasser).
R1–X + R2–Y
- Zwei Ethanol-Moleküle reagieren zu Diethylether und Wasser
- Esterreaktion von Essigsäure mit Ethylalkohol zu Essigsäureethylester
- Veresterung von Glycerin zu einem Fett
- Veresterung der Benzoesäure mit Methylalkohol zu Benzoesäuremethylester
- Polykondensation von Hexamethylendiamin und Adipinsäure zu Polyamid 6.6
- Polykondensation von Terephthalsäure und Ethylenglycol zu einem Polyester
Kettenpolymerisationen
Monomere reagieren in einer Kettenwachstumsreaktion zu einem Polymer.
- Ethen polymerisiert zu Polyethen
- Styrol polymerisiert zu Polystyrol
- Vinylchlorid polymerisiert zu PVC
Polyadditionen
Mehrere Monomere lagern sich unter Umlagerung aneinander.
Hydrierungen
Eine Hydrierung ist eine Reduktion, bei der ein Stoff durch Reaktion mit Wasserstoff Elektronen aufnimmt; dabei werden Wasserstoff-Atome in seine Struktur eingebaut.
- Herstellen von Methanol aus Synthesegas
- Hydrierung von Nitrobenzol zu Anilin
- Hydrierung bei der Fetthärtung
- D-Fructose wird zu Sorbit hydriert
Oxidationen
Bei einer Oxidation (nach Lavoisier) wird Sauerstoff in eine Verbindung eingeführt. Eine Oxidation liegt auch vor, wenn Elektronen entzogen werden und sich die Oxidationszahl erhöht.
- Oxidation eines primären Alkohols zu einem Aldehyd
- Oxidation eines sekundären Alkohols zu einem Keton
- Oxidation von Methylalkohol zu Methanal
- Oxidation von Cyclohexan zu Cyclohexanol
- Oxidation von Toluol zur Benzoesäure
Säure-Base-Reaktionen
Brønsted-Säuren oder Brønsted-Basen nehmen Protonen auf oder geben sie ab.
Grignard-Reaktionen
Bei den nach Victor Grignard (1871–1935) benannten Reaktionen wird ein metallorganisches Reagenz zur Synthese neuer, organischer Verbindungen eingesetzt.