Im Jahr 1930 war die Polymerisation von Styrol zu Polystyrol gelungen. Mit dem
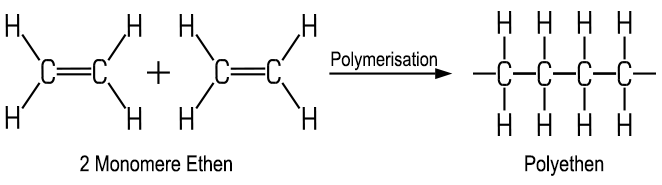
einfachsten Alken, dem Ethen, gelang
die Polymerisation zunächst nicht, da der gasförmige Zustand
des Ethens ein Hindernis darstellte. 1933 stellte ein Forscher-Team bei
der britischen Firma ICI unter 1400 Bar Druck erstmals Polyethen
dar. Sieben Jahre später gelang es mit einer veränderten Apparatur,
das Ethen wirtschaftlich rentabel zu polymerisieren. Nach diesem Verfahren
wird das dabei entstehende Hochdruck-Polyethen noch heute hergestellt. Seine Dichte beträgt 0,93 g/cm³, es ist
relativ zäh und elastisch. Aufgrund seiner niedrigen Dichte wird es
auch als LDPE abgekürzt (engl. low density polyethen). Da es
schon bei 98 °C schmilzt, ist es für Gegenstände, die mit
heißem Wasser in Berührung kommen, nicht brauchbar. Es eignet
sich zur Herstellung von Verpackungsfolien, Tragetaschen und Getränkeflaschen.
Im Jahre 1953 entwickelte der deutsche
Chemiker Karl Ziegler (1898–1973) ein Verfahren, bei dem das Ethen bei
niedrigem Druck polymerisiert. Die Herstellung gelingt bei 60 Bar und einer
Temperatur von 60 bis 240 °C unter Zuhilfenahme von Titan- oder Magnesium-Katalysatoren.
Man erhält ein unlösliches Pulver, das später zu einem Granulat
verarbeitet wird. Das entstehende Niederdruck-Polyethen (Abkürzung HDPE = high density polyethen) hat eine Dichte von
0,94 bis 0,97 g/cm³. Dieses Polyethen besitzt einen höheren Schmelzpunkt
und ist belastbarer. Der italienische Chemiker Giulio Natta (1903–1979)
entwickelte die von Ziegler eingesetzten Katalysatoren weiter. Ziegler
und Natta erhielten im Jahre 1963 für die Entwicklung der Ziegler-Natta-Katalysatoren den Nobelpreis für Chemie. Es handelt sich dabei um metallorganische
Verbindungen, die bei Normaldruck Polymerisationen katalysieren. Polyethen zeichnet sich durch eine ausgezeichnete
Beständigkeit gegen Wasser, Säuren, Laugen und den meisten organischen
Lösungsmitteln bis zu einer Temperatur von 60 °C aus. Es gehört zu den Thermoplasten und lässt sich daher gut in Spritz- und Gießverfahren verarbeiten.
Setzt man Ethen einem Druck von 1400 bis 3500 Bar und Temperaturen von 150 bis 350 °C aus und
gibt man Spuren von reinem Sauerstoff zu, dann
entsteht Hochdruck-Polyethen. Der Sauerstoff bildet Radikale und wirkt
als Initiator, so dass das Ethen zu langen Ketten polymerisiert. Meistens entstehen dabei auch verzweigte
Ketten. Beim Niederdruck-Polyethen gelingt die Reaktion bereits bei niedrigem
Druck unter Zusatz der Ziegler-Natta-Katalysatoren.
Aufgrund seiner niedrigen Dichte und seiner hohen
Stabilität wird Polyethen in vielen Haushaltsgegenständen und
in Kinderspielzeug eingesetzt.
Auch Trinkwasser-Rohre und Kabel-Isolierungen bestehen aus
Polyethen. Schädliche
Wirkungen auf die Gesundheit sind momentan nicht bekannt,
allerdings ist
es gegen Umwelteinflüsse widerstandsfähig und baut
sich in der
Natur schlecht ab. Daher ist ein Recycling des Kunststoffs sinnvoll.