Traditionelle Seifenherstellung nach der Neutralölverseifung
Früher war die traditionelle
Seifenherstellung ein sehr aufwändiges Verfahren, die genauen
Rezepte waren gut gehütete Geheimnisse. Der Import von Kokosfett
nach Europa ab 1830 und das Ermöglichen der industriellen Produktion
von Soda nach dem Verfahren von Solvay
(1861) leitete das Zeitalter der modernen Waschmittel ein.
Bei
der Neutralölverseifung von Fetten
mit Natronlauge verläuft die
Reaktion relativ langsam. Der Prozess benötigt viel Zeit. Beim traditionellen
Kaltverfahren ist er erst nach sechs Wochen vollständig abgeschlossen.
Im folgenden Beispiel reagiert das Natriumhydroxid mit einem Fett-Molekül,
das aus einem Ölsäure-Rest, einem Palmitinsäure-Rest und
einem Linolsäure-Rest aufgebaut ist. Das Fett-Molekül spaltet
sich auf und man erhält Glycerin, sowie die drei entsprechenden Fettsäuresalze
Natriumoleat, Natriumpalmitat und Natriumlinolat. Diese Salze sind typische
Bestandteile einer Seife.
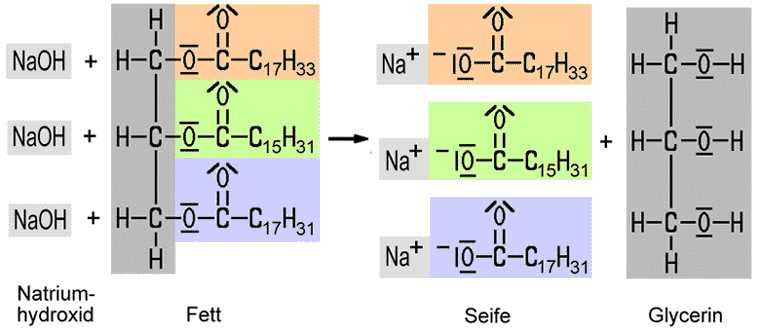
| Prinzip der Verseifung | |
| |
| Verseifung eines Fett-Moleküls, das aus einem Öl-, Palmitin- und Linolsäure-Rest aufgebaut ist. |
Beim
Heißverfahren findet dieser
Prozess stark beschleunigt bei höheren Temperaturen statt. Durch das
nachfolgende Aussalzen mit
Natriumchlorid wird die Löslichkeit des entstandenen Seifenleims
herabgesetzt. Dadurch scheidet sich der Seifenkern als feste und oben schwimmende
Schicht ab. In der Unterlauge verbleibt das Glycerin,
das für andere Produkte als Rohstoff dient.
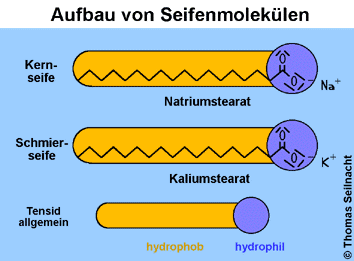
Die aus Natronlauge und
Fett hergestellte Kernseife ist noch stark
alkalisch. Aus diesem Grund wird der Vorgang des Aussalzens mehrfach wiederholt.
Verwendet man zur Verseifung des Fetts Kalilauge statt Natronlauge erhält man beim Aussalzen eine halbfeste bis flüssige
Masse, die Schmierseife. Schmierseifen werden
vor allem zu Reinigungszwecken in Haushalten eingesetzt, Kernseifen für
die Fleckentfernung oder zum Verfilzen von Stoffen.
 |
|
Großtechnische
Seifenherstellung nach der Fettsäureverseifung
Die traditionellen Verfahren werden heute bei den großtechnischen Prozessen kaum noch angewendet. Stattdessen spaltet man zunächst die Fette und Öle in Druckkesseln bei 180 °C durch eine Hydrolyse mit Wasserdampf zu freien Fettsäuren. Das gleichzeitig entstehende Glycerin wird abgetrennt. Die Fettsäurereinigung erfolgt durch eine anschließende Vakuumdestillation bei niedrigem Druck. Beim Einrühren der Fettsäuren in eine siedende Natriumcarbonat-Lösung (Soda-Lösung) reagieren die Fettsäuren mit dem Natriumcarbonat zu Seife, Wasser und Kohlenstoffdioxid.
Die traditionellen Verfahren werden heute bei den großtechnischen Prozessen kaum noch angewendet. Stattdessen spaltet man zunächst die Fette und Öle in Druckkesseln bei 180 °C durch eine Hydrolyse mit Wasserdampf zu freien Fettsäuren. Das gleichzeitig entstehende Glycerin wird abgetrennt. Die Fettsäurereinigung erfolgt durch eine anschließende Vakuumdestillation bei niedrigem Druck. Beim Einrühren der Fettsäuren in eine siedende Natriumcarbonat-Lösung (Soda-Lösung) reagieren die Fettsäuren mit dem Natriumcarbonat zu Seife, Wasser und Kohlenstoffdioxid.
2 C17H35COOH + Na2CO3
Stearinsäure + Natriumcarbonat
Der Vorteil der Fettsäureverseifung
besteht auch darin, dass man aus Erdöl Seife herstellen kann. Die
aus dem Erdöl gewonnenen langkettigen Paraffine lassen sich zunächst
durch eine katalytische Oxidation in Fettsäuren umwandeln. Auf diese
Art und Weise kann auch aus Stearinsäure
Seife hergestellt werden. Stearinsäure ist ein Bestandteil des Kerzenwachses.
C17H35COOH
+ NaOH Stearinsäure + Natriumhydroxid
Allerdings stehen momentan
genügend natürliche Fette und Öle zur Verfügung, so
dass die Herstellung von Seifen aus Erdöl eher unbedeutend ist.
Großtechnische Herstellung der Tenside
Die Herstellungsverfahren
der modernen Tenside verlaufen in vielen,
komplizierten Schritten. Der „klassische“ Weg zur Herstellung eines Alkylbenzolsulfonats
erfolgt aus den aus Erdöl gewonnenen
Paraffinen. Diese werden in einer
Substitutionsreaktion mit
Chlor zu Chloralkanen umgesetzt (I).
Die dabei erhaltenen Chloralkane lassen sich mit Platin- oder Aluminiumkatalysatoren
bei hoher Temperatur zu linearen Alkenen
dehydrieren. Bei der hier stattfindenden Eliminierungsreaktion entsteht
auch Chlorwasserstoff (II).
Mit Hilfe eines Friedel-Crafts-Katalysators wie Fluorwasserstoff
erhält man mit Benzol ein Alkylbenzol
(III).
(I) Alkan + Chlor
(II) Chloralkan
(III) Alken + Benzol
Mit Schwefeltrioxid, das zum Beispiel bei der Schwefelsäureherstellung anfällt, lässt
sich in einer Sulfonierung die Sulfo-Gruppe -SO3H
in ein Alkylbenzol-Molekül einführen. Man verwendet eine
Lösung von Schwefeltrioxid in konzentrierter Schwefelsäure
(Oleum).
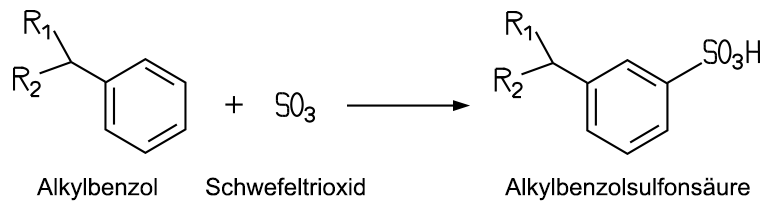
| Prinzip einer Sulfonierung | |
| |
| Die Sulfonierung des Aromaten durch das elektrophile Schwefeltrioxid ist eine elektrophile Substitution. |
Das Wasserstoff-Atom der
Sulfo-Gruppe SO3H kann ein Proton abgegeben, die Alkylbenzolsulfonsäure
ist daher eine Säure. So lässt
sich die Sulfonsäure auch mit Natronlauge
neutralisieren, und man erhält das Salz der Sulfonsäure, ein Alkylbenzolsulfonat:
R-SO3H + NaOH R-SO3−Na+ + H2O
(R=Alkylbenzol)
R-SO3−Na+ + H2O
(R=Alkylbenzol)
Alkylbenzolsulfonsäure + Natriumhydroxid Alkylbenzolsulfonat + Wasser
Alkylbenzolsulfonat + Wasser
Andere Tenside wie die Fettalkoholsulfate (FAS) oder die Alkylpolyglucoside (APG) lassen sich aus nachwachsenden Rohstoffen gewinnen. Beide sind biologisch sehr gut abbaubar. Die dafür notwendige Glucose kann aus der Stärke von Mais- oder Kartoffelpflanzen gewonnenen werden oder direkt aus zuckerliefernden Pflanzen wie Zuckerrohr oder Zuckerrüben. Das ebenfalls notwendige Kokosfett wird über den Zwischenschritt einer Ester-Reaktion zu Fettalkohol reduziert. Man bezeichnet einen primären Alkohol mit 6 bis 22 Kohlenstoff-Atomen, wenn er aus Fetten oder Fettsäuren hergestellt wurde, als Fettalkohol:
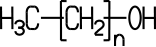
Aufbau eines Fettalkohols
Die Alkylpolyglucoside (APG) lassen sich durch Substitution eines Fettalkohols mit Glucose mit Hilfe eines geeigneten Katalysators herstellen. Durch ständiges Entfernen des bei der Reaktion entstehenden Wassers und durch die Zugabe von Fettalkohol im Überschuss verschiebt sich die Gleichgewichtsreaktion nach rechts:
R-SO3H + NaOH
Alkylbenzolsulfonsäure + Natriumhydroxid
Andere Tenside wie die Fettalkoholsulfate (FAS) oder die Alkylpolyglucoside (APG) lassen sich aus nachwachsenden Rohstoffen gewinnen. Beide sind biologisch sehr gut abbaubar. Die dafür notwendige Glucose kann aus der Stärke von Mais- oder Kartoffelpflanzen gewonnenen werden oder direkt aus zuckerliefernden Pflanzen wie Zuckerrohr oder Zuckerrüben. Das ebenfalls notwendige Kokosfett wird über den Zwischenschritt einer Ester-Reaktion zu Fettalkohol reduziert. Man bezeichnet einen primären Alkohol mit 6 bis 22 Kohlenstoff-Atomen, wenn er aus Fetten oder Fettsäuren hergestellt wurde, als Fettalkohol:
Aufbau eines Fettalkohols
Die Alkylpolyglucoside (APG) lassen sich durch Substitution eines Fettalkohols mit Glucose mit Hilfe eines geeigneten Katalysators herstellen. Durch ständiges Entfernen des bei der Reaktion entstehenden Wassers und durch die Zugabe von Fettalkohol im Überschuss verschiebt sich die Gleichgewichtsreaktion nach rechts:
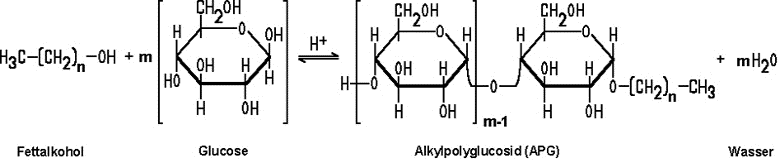
| Herstellen eines Alkylpolyglucosides (AGP) | |
| |
| Die Herstellung erfolgt aus einem Fettalkohol und Glucose. |
Zur Herstellung eines Fettalkoholsulfates
(FAS) kann man zum Beispiel den Fettalkohol Dodecanol mit wenig
konzentrierter Schwefelsäure versetzen und schwach erwärmen. Nach
einigen Minuten entsteht ein gelber Ester. Mit Natronlauge
wird neutralisiert. Dass ein Tensid
entstanden ist, lässt sich an der Schaumbildung nachweisen, wenn das Produkt zusammen mit
Wasser geschüttelt wird. Bei der Umsetzung des Fettalkohols mit konzentrierter Schwefelsäure bildet sich zunächst ein Ester:
CH3-(CH2)n-OH + H2SO4
Fettalkohol + Schwefelsäure
Bei der Neutralisation
des Esters mit der Natronlauge, entsteht ein Fettalkoholsulfat:
CH3-(CH2)n-O-SO3H + NaOH
Schwefelsäurealkylester + Natronlauge
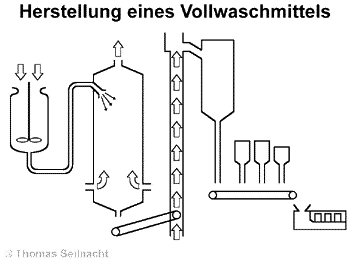
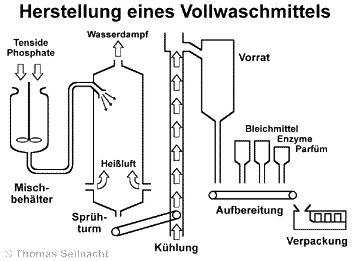
Die frühen Vollwaschmittel
kamen in Pulverform auf den Markt. Erwünscht waren vor allem eine
gute Lager-, Transport- und Dosierfähigkeit. Beim Hochdrucksprühverfahren
werden die festen und flüssigen Komponenten des Waschmittels in einem
Mischbehälter mit Wasser vermischt, so
dass ein pumpfähiger Brei entsteht. Im Sprühturm
trocknen die Komponenten durch das Zugeben von Heißluft bei etwa 300 °C.
Dabei entsteht ein Pulver, das sehr gut wasserlöslich ist und wenig
stäubt. Auf dem nachfolgenden Transportband wird die Kühlung
vorgenommen. Dann wird es im Vorratsbehälter gelagert. Erst danach gibt man zur Aufbereitung die
temperaturempfindlichen Bestandteile wie Bleichmittel, Enzyme oder Parfüms
hinzu. Im Verpackungsautomat wird das fertige
Waschmittel für die Lagerung und den Verkauf portioniert und abgepackt. Das Produktionsschema ist vereinfacht wiedergegeben:
 |
 |
Bei den Kompaktwaschmitteln
wird das aus dem Sprühturm kommende Pulver zusammen mit den nachträglich
zugegebenen Komponenten verdichtet. Man erhält ein Granulat mit höherer
Schüttdichte. Zur Herstellung von Tabs presst man das Granulat zu
Tabletten. Hierbei ist es auch möglich, mehrschichtige Tabs herzustellen.
In der oberen Schicht befinden sich dann empfindliche Komponenten wie die
Bleichmittel und in der unteren Bleichaktivatoren und Enzyme.