Elektronegativität
Die von Linus
Pauling im Jahr 1932 eingeführte Maßzahl der Elektronegativität
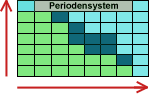
(EN) gibt an, wie gerne ein Atom Bindungselektronen an sich zieht. Die
EN nimmt im Periodensystem tendenziell von links unten nach rechts oben
zu. Die Fluor-Atome sind am elektronegativsten, wenn man die Edelgase nicht berücksichtigt,
die Atome der Alkalimetalle sind
am wenigsten elektronegativ. Als grobe Faustregel gilt: Beträgt die Differenz der EN zwischen
zwei Atomen mehr als 1,7, bilden sie eine Ionenbindung,
dann geben die weniger elektronegativen Atome ihre Valenzelektronen
an die elektronegativeren Atome ab. Es entsteht ein Salz.
Dies findet in der Regel zwischen einem Metall
und einem Nichtmetall statt. Bei kleineren EN-Differenzen benutzen nichtmetallische
Bindungspartner gemeinsam das bindende Elektronenpaar zur Elektronenpaarbindung.
Atome
mit hoher Elektronegativität
|
Atomsorte
|
EN nach Pauling
|
|
Fluor
|
3,98
|
|
Sauerstoff
|
3,44
|
|
Chlor
|
3,16
|
|
Stickstoff
|
3,04
|
|
Brom
|
2,96
|
|
Iod
|
2,66
|
|
Xenon
|
2,60
|
|
Schwefel
|
2,58
|
|
Kohlenstoff
|
2,55
|
|
Selen
|
2,55
|
|
Wasserstoff
|
2,20
|
|
Phosphor
|
2,19
|
|
Arsen
|
2,18
|
Atome mit
niedriger Elektronegativität
|
Atomsorte
|
EN nach Pauling
|
|
Francium
|
0,70
|
|
Caesium
|
0,79
|
|
Rubidium
|
0,82
|
|
Kalium
|
0,82
|
|
Barium
|
0,89
|
|
Radium
|
0,90
|
|
Natrium
|
0,93
|
|
Strontium
|
0,95
|
|
Lithium
|
0,98
|
|
Calcium
|
1,00
|
|
Actinium
|
1,10
|
|
