105,989 g/mol
286,142 g/mol
keine Angaben
2,54 g/cm3
1,46 g/cm3
+856 °C
100g H2O lösen 21,4 g (L) (wasserfrei)
100g H2O lösen 21,66 g (L) (Decahydrat)
Wasserfrei
Weißes Pulver
Decahydrat
Kristallines Pulver
Wasserfreies Natriumcarbonat ist ein weißes Pulver, das Haut und Schleimhäute reizt. Es ist stark hygroskopisch und nimmt Feuchtigkeit aus der Luft auf. Beim Erwärmen auf 40 °C nimmt die Löslichkeit des wasserfreien Natriumcarbonats zunächst zu, sie nimmt dann aber beim weiteren Erwärmen wieder leicht ab:
Wasserlöslichkeit (L): 100g H2O lösen x g Natriumcarbonat wasserfrei
0 °C
|
20 °C
|
40 °C
|
60 °C
|
80 °C
|
100 °C |
7,1 g
|
21,4 g
|
48,5 g
|
46,5 g
|
45,8 g
|
45,5 g |
Beim Lösen im Wasser entsteht unter Wärmeentwicklung eine stark alkalische Lösung. Das Carbonat-Ion reagiert dabei als
Base mit einem Wasser-Molekül zu einem Hydrogencarbonat-Ion und einem Hydroxid-Ion:
CO
32− + H
2O
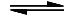
HCO
3− + OH
− 
Ein angefeuchtetes Universalindikator-Papier färbt sich mit Natriumcarbonat blau.
Mit einer starken
Säure entwickelt Natriumcarbonat unter Aufbrausen das Gas
Kohlenstoffdioxid und die entsprechenden Salze der Säure. Mit Salzsäure entstehen Natriumchlorid, Kohlenstoffdioxid und Wasser. Mit Schwefelsäure erhält man Natriumsulfat, Kohlenstoffdioxid und Wasser:
Na
2CO
3 + 2 HCl

2 NaCl + H
2O + CO
2Na
2CO
3 + H
2SO
4 
Na
2SO
4 + H
2O + CO
2 Verdünnte Salzsäure reagiert mit Natriumcarbonat unter Aufschäumen.
Verdünnte Salzsäure reagiert mit Natriumcarbonat unter Aufschäumen.
Wasserfrei: Na
2CO
3
Monohydrat: Na
2CO
3 • H
2O
Heptahydrat: Na
2CO
3 • 7 H
2O
Decahydrat: Na
2CO
3 • 10 H
2O
Eine Gewinnung aus dem Natriumcarbonat-Mineral Natrit lohnt sich nicht, weil das Mineral sehr selten vorkommt. Natriumcarbonat aus Natronseen – beispielsweise aus dem Owens Lake in den USA – kann durch Verdunsten von Wasser gewonnen werden. Die natürlichen Heilquellen in Karlsbad enthalten ebenfalls hohe Soda-Konzentrationen. Im Labor kann man Natriumcarbonat durch Einleiten von
Kohlenstoffdioxid in
Natronlauge herstellen:
2 NaOH + CO
2 + H
2O

Na
2CO
3 + 2 H
2O
In der chemischen Industrie wird es heute hauptsächlich nach dem Solvay-Verfahren aus Kochsalz und
Kalk hergestellt. Zuerst setzt man Sole (stark salzhaltiges Wasser) mit
Ammoniak NH
3 und
Kohlenstoffdioxid CO
2 in einem Reaktionsofen zu
Natriumhydrogencarbonat um:
NaCl + H
2O + NH
3 + CO
2 
NaHCO
3 + NH
4Cl
Durch Calcinieren, einem Erhitzen auf 200 °C, wird das Natriumhydrogencarbonat danach in das Carbonat umgewandelt:
2 NaHCO
3 
Na
2CO
3 + H
2O + CO
2
Bei dem alten Verfahren nach Nicolas Leblanc (1742–1806) erhielt man Soda aus
Natriumchlorid,
Schwefelsäure und
Natriumsulfat. Das Verfahren wurde aufgrund eines Preisausschreibens der Pariser Akademie der Wissenschaften von dem französischen Fabrikanten und Privatgelehrten Leblanc entwickelt. Zunächst stellte er aus Natriumchlorid und Schwefelsäure Natriumsulfat her. Beim Erhitzen von Natriumsulfat zusammen mit Kalk und Kohle entstand Soda, Calciumsulfid und Kohlenstoffdioxid:
Na
2SO
4 + CaCO
3 + 2 C

Na
2CO
3 + CaS + 2 CO
2
Das entstehende Soda wurde danach mit Wasser ausgelaugt. Der Nachteil des Verfahrens bestand in den hohen Energiekosten und im Anfall unerwünschter Abfallprodukte. Das Verfahren ist heute nur noch von historischer Bedeutung, es leitete aber den Beginn der chemischen Industrie ein.
Natriumcarbonat wird in großem Umfang von der Glasindustrie verwendet: Die Zugabe verhindert das Auskristallisieren der Schmelze beim Erstarren der Glasschmelze. Dadurch erhält man amorphes, sehr homogenes und durchsichtiges Glas. Die Konzentration bestimmt auch die Fließfähigkeit der Schmelze. In der chemischen Industrie ist Natriumcarbonat ein wichtiges Zwischenprodukt für andere Natrium-Verbindungen, beispielsweise zur Herstellung von
Natriumhydroxid,
Natriumhydrogencarbonat oder
Ultramarinblau. Die Zellstoff- und Papierindustrie setzt das Carbonat zum Aufschluss, zur Neutralisation, zum Reinigen, zum Bleichen, sowie zur Aufbereitung von Altpapier ein. Bei der Eisenverhüttung wird es bei der Entschwefelung von Roheisen und Stahl und als Flotations- und Flussmittel eingesetzt. Weiterhin dient es zum Enthärten von Wasser, wasserfreies Natriumcarbonat eignet sich auch als Trocknungsmittel für Räume. Die glänzende Oberfläche beim Laugengebäck wird durch das Behandeln mit Soda erreicht. Weitere Verwendungen sind bei der Leder-, Keramik- und Textilindustrie zu finden.
Natriumcarbonat wird heute noch zur
Waschmittelherstellung verwendet. Im Jahr 1878 kam „Henkels Bleichsoda“ auf den Markt, ein Gemisch aus Soda und Natriumsilicat im Verhältnis 4 zu 1. Es diente zum Herstellen einer Waschlauge und zum Enthärten des Wassers. Die heutigen Waschmittel enthalten Tenside, die nicht mehr einen so hohen pH-Wert haben und das Textilgewebe besser schonen.
Weitere Infos
Infos zur
Kohlensäure und zu den
Carbonaten
Infos zu den
Waschmitteln
Forschungsauftrag:
Unbekannter Stoff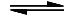 HCO3− + OH−
HCO3− + OH− 
 2 NaCl + H2O + CO2
2 NaCl + H2O + CO2 Na2SO4 + H2O + CO2
Na2SO4 + H2O + CO2