Stickstoffdioxid
NO2
CAS 10102-44-0
Stickstoffdioxid
Nitrogen dioxide
46,006 g/mol
0,5 ml/m3 oder 950 µg/m3 (TRGS 900)
3,663 g/l (Gas, 0 °C, 1013 hPa) (Stickstoffdioxid zu Luft = 2,84)
−9,3 °C
+21,15 °C
Bildung von Salpetersäure
0,5 ml/m3 oder 950 µg/m3 (TRGS 900)
3,663 g/l (Gas, 0 °C, 1013 hPa) (Stickstoffdioxid zu Luft = 2,84)
−9,3 °C
+21,15 °C
Bildung von Salpetersäure
Braunrotes Gas mit brenzligem Geruch (an Chlor erinnernd)



Gefahrenklassen + Kategorie
Oxidierendes Gas 1
Gase unter Druck, verdicht. Gas
Akute Toxizität inhalativ 1
Schwere Augenschädigung 1
Ätzwirkung auf die Haut 1B
Oxidierendes Gas 1
Gase unter Druck, verdicht. Gas
Akute Toxizität inhalativ 1
Schwere Augenschädigung 1
Ätzwirkung auf die Haut 1B
HP-Sätze (siehe Hinweis)
H 270, 280, 314, 318, 330, EUH071
P 220, 260, 280.1-3+6+7, 304+340+315, 305+351+338+310
Entsorgung besondere Hinweise
H 270, 280, 314, 318, 330, EUH071
P 220, 260, 280.1-3+6+7, 304+340+315, 305+351+338+310
Entsorgung besondere Hinweise
Aufgrund der stark toxischen Wirkung wird von Experimenten zur Herstellung des Gases an Schulen abgeraten. Für Experimente, bei denen die Gefahr besteht, dass geringe Mengen Stickstoffdioxid frei werden, ist ein Abzug notwendig. Werdende oder stillende Mütter dürfen mit diesem Stoff nicht arbeiten. Gasflaschen mit Stickstoffdioxid an Schulen nicht aufbewahren!
Wirkung auf den menschlichen Körper
Stickstoffdioxid ist ein stark toxisches Gas. Der Arbeitsplatzgrenzwert liegt bei 950 µg/m³ oder bei 0,5 ml/m³ (=0,5 ppm Volumenanteile). Je nach Person treten ab einer Konzentration von 1 bis 13 ppm Reizungen an den Schleimhäuten der Atemwege auf. Die Augen werden ab 10 ppm gereizt. 100 ppm in der Atemluft wirken nach einer Stunde tödlich. Die akute Vergiftung durch Inhalation beginnt mit Schwindel und Kopfschmerzen, ein auftretendes Lungenödem kann auch noch nach Tagen zum Tod führen. Als Gegenmaßnahmen sind absolute Körperruhe, ärztliche Behandlung und Sauerstoff-Beatmung notwendig. Eine ärztliche Beobachtung ist mindestens zwei Tage lang erforderlich. Chronische Wirkungen auf die Atemwege sind ab 1 ppm dokumentiert. Stickstoffdioxid ist im Zigarettenrauch enthalten. Es entsteht bei der Verfeuerung fossiler Brennstoffen wie Benzin oder Diesel und befindet sich in den Abgasen.

Rauchende Salpetersäure setzt Stickstoffdioxid frei.
Chemisch-physikalische Eigenschaften
Stickstoffdioxid ist ein braunrotes Gas, das bei +21,2 °C zu einer braunen Flüssigkeit kondensiert. Bei weiterem Abkühlen verschwindet die braune Farbe allmählich, bei −11,2 °C erstarrt die Flüssigkeit zu farblosen Kristallen. Unterhalb von 0 °C wandeln sich alle Stickstoffdioxid-Moleküle in Distickstofftetroxid-Moleküle um, es entsteht das farblose Dimer N2O4:
Das chemische Gleichgewicht dieser Reaktion ist temperaturabhängig. Bei steigender Temperatur verschiebt sich das Gleichgewicht nach links. Bei +64 °C ist es etwa ausgeglichen. Daher kommen bei Zimmertemperatur die beiden Gase immer in einem Gemisch vor. Erst bei +150 °C liegt reines Stickstoffdioxid vor.

Im mit Eiswasser gekühlten Rundkolben (Bild links) liegt hauptsächlich das Dimer N2O4 vor;
in dem mit heißem Wasser erwärmten Rundkolben (Bild rechts) findet sich überwiegend NO2.
Film
Oberhalb von 150 °C beginnt ein Zerfall in Stickstoffmonooxid und Sauerstoff:
Bei 620° C liegt das chemische Gleichgewicht dieser Reaktion ganz auf der rechten Seite, und das Gas ist vollständig zerfallen. Aufgrund der Bereitschaft, Sauerstoff-Atome abgeben zu können, wirkt Stickstoffdioxid als starkes Oxidationsmittel. Kohle, Phosphor und Schwefel verbrennen, Kohlenstoffmonooxid oxidiert zu Kohlenstoffdioxid, Schwefelwasserstoff zu Schwefel und Wasser. Mit Schwefelwasserstoff und halogenierten Kohlenwasserstoffen entstehen explosionsgefährliche Gemische. Bei der Reaktion mit Wasser bildet sich Salpetersäure. Diese Reaktion dient im Ostwald-Verfahren zur Herstellung von Salpetersäure:
Stickstoffdioxid ist ein stark toxisches Gas. Der Arbeitsplatzgrenzwert liegt bei 950 µg/m³ oder bei 0,5 ml/m³ (=0,5 ppm Volumenanteile). Je nach Person treten ab einer Konzentration von 1 bis 13 ppm Reizungen an den Schleimhäuten der Atemwege auf. Die Augen werden ab 10 ppm gereizt. 100 ppm in der Atemluft wirken nach einer Stunde tödlich. Die akute Vergiftung durch Inhalation beginnt mit Schwindel und Kopfschmerzen, ein auftretendes Lungenödem kann auch noch nach Tagen zum Tod führen. Als Gegenmaßnahmen sind absolute Körperruhe, ärztliche Behandlung und Sauerstoff-Beatmung notwendig. Eine ärztliche Beobachtung ist mindestens zwei Tage lang erforderlich. Chronische Wirkungen auf die Atemwege sind ab 1 ppm dokumentiert. Stickstoffdioxid ist im Zigarettenrauch enthalten. Es entsteht bei der Verfeuerung fossiler Brennstoffen wie Benzin oder Diesel und befindet sich in den Abgasen.
Rauchende Salpetersäure setzt Stickstoffdioxid frei.
Chemisch-physikalische Eigenschaften
Stickstoffdioxid ist ein braunrotes Gas, das bei +21,2 °C zu einer braunen Flüssigkeit kondensiert. Bei weiterem Abkühlen verschwindet die braune Farbe allmählich, bei −11,2 °C erstarrt die Flüssigkeit zu farblosen Kristallen. Unterhalb von 0 °C wandeln sich alle Stickstoffdioxid-Moleküle in Distickstofftetroxid-Moleküle um, es entsteht das farblose Dimer N2O4:
2 NO2 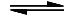 N2O4 ΔHR = −57 kJ/mol
N2O4 ΔHR = −57 kJ/mol
Das chemische Gleichgewicht dieser Reaktion ist temperaturabhängig. Bei steigender Temperatur verschiebt sich das Gleichgewicht nach links. Bei +64 °C ist es etwa ausgeglichen. Daher kommen bei Zimmertemperatur die beiden Gase immer in einem Gemisch vor. Erst bei +150 °C liegt reines Stickstoffdioxid vor.

Im mit Eiswasser gekühlten Rundkolben (Bild links) liegt hauptsächlich das Dimer N2O4 vor;
in dem mit heißem Wasser erwärmten Rundkolben (Bild rechts) findet sich überwiegend NO2.
Film
Oberhalb von 150 °C beginnt ein Zerfall in Stickstoffmonooxid und Sauerstoff:
2 NO2 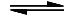 2 NO + O2 ΔHR = +114 kJ/mol
2 NO + O2 ΔHR = +114 kJ/mol
Bei 620° C liegt das chemische Gleichgewicht dieser Reaktion ganz auf der rechten Seite, und das Gas ist vollständig zerfallen. Aufgrund der Bereitschaft, Sauerstoff-Atome abgeben zu können, wirkt Stickstoffdioxid als starkes Oxidationsmittel. Kohle, Phosphor und Schwefel verbrennen, Kohlenstoffmonooxid oxidiert zu Kohlenstoffdioxid, Schwefelwasserstoff zu Schwefel und Wasser. Mit Schwefelwasserstoff und halogenierten Kohlenwasserstoffen entstehen explosionsgefährliche Gemische. Bei der Reaktion mit Wasser bildet sich Salpetersäure. Diese Reaktion dient im Ostwald-Verfahren zur Herstellung von Salpetersäure:
3 NO2 + H2O  2 HNO3 + NO
2 HNO3 + NO
Im Labor kann man Stickstoffdioxid durch vorsichtiges Erhitzen von Blei(II)-nitrat erhalten:
Das Gas entsteht auch, wenn man Metalle in konzentrierter Salpetersäure auflöst, beispielsweise bei der Reaktion von Salpetersäure mit Kupfer. Das dabei gebildete Stickstoffmonooxid NO reagiert sofort mit der Luft weiter zu Stickstoffdioxid.
Stickstoffdioxid kann auch durch einen Lichtbogen an einer Hochspannung hergestellt werden. Nach dem 1903 entwickelten Verfahren von Birkeland und Eyde wird Salpetersäure gewonnen, wenn das hierbei entstehende Stickstoffdioxid in Wasser geleitet wird.
Die industrielle Gewinnung durch die Oxidation von Ammoniak wurde von Wilhelm Ostwald entwickelt. Die Produktion des Ammoniaks erfolgt nach dem Haber-Bosch-Verfahren. Das so gewonnene Ammoniak wird mit Luft vermischt und in einem Reaktor bei 800 °C und einem Platin-Rhodium-Katalysator zu Stickstoffmonooxid und Wasser oxidiert:
In einem nachgeschalteten Reaktor reagiert das Stickstoffmonooxid mit Sauerstoff in einer weiteren Oxidation zu Stickstoffdioxid. Diese Reaktion ist erst bei Temperaturen unterhalb 50 °C durchführbar:
2 Pb(NO3)2 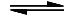 2 PbO + 4 NO2 + O2
2 PbO + 4 NO2 + O2
Das Gas entsteht auch, wenn man Metalle in konzentrierter Salpetersäure auflöst, beispielsweise bei der Reaktion von Salpetersäure mit Kupfer. Das dabei gebildete Stickstoffmonooxid NO reagiert sofort mit der Luft weiter zu Stickstoffdioxid.
3 Cu + 8 HNO3  3 Cu(NO3)2 + 4 H2O + 2 NO
3 Cu(NO3)2 + 4 H2O + 2 NO
Stickstoffdioxid kann auch durch einen Lichtbogen an einer Hochspannung hergestellt werden. Nach dem 1903 entwickelten Verfahren von Birkeland und Eyde wird Salpetersäure gewonnen, wenn das hierbei entstehende Stickstoffdioxid in Wasser geleitet wird.
Die industrielle Gewinnung durch die Oxidation von Ammoniak wurde von Wilhelm Ostwald entwickelt. Die Produktion des Ammoniaks erfolgt nach dem Haber-Bosch-Verfahren. Das so gewonnene Ammoniak wird mit Luft vermischt und in einem Reaktor bei 800 °C und einem Platin-Rhodium-Katalysator zu Stickstoffmonooxid und Wasser oxidiert:
4 NH3 + 5 O2  4 NO + 6 H2O ΔHR = −908 kJ
4 NO + 6 H2O ΔHR = −908 kJ
In einem nachgeschalteten Reaktor reagiert das Stickstoffmonooxid mit Sauerstoff in einer weiteren Oxidation zu Stickstoffdioxid. Diese Reaktion ist erst bei Temperaturen unterhalb 50 °C durchführbar:
2 NO + O2  2 NO2 ΔHR = −114 kJ/mol
2 NO2 ΔHR = −114 kJ/mol
Stickstoffdioxid dient vor allem zur Herstellung von Salpetersäure. Es kann als Oxidationsmittel verwendet werden, daher eignet es sich als Komponente für Raketentreibstoffe. Im Gemisch mit Nitrobenzol erhält man den brisanten Sprengstoff Panclastit.
Weitere Infos und Medien
Das Auto und seine Abgase
Das Ostwald-Verfahren zur Herstellung von Salpetersäure
Weitere Infos und Medien
Das Auto und seine Abgase
Das Ostwald-Verfahren zur Herstellung von Salpetersäure
© Thomas Seilnacht / Benutzerhandbuch / Lizenzbestimmungen / Impressum / Datenschutz / Literaturquellen

