Ethylenglycol, Glykol
C2H4(OH)2
Ethylenglycol, Glykol
Ethan-1,2-diol
1,2-Ethandiol
Ethan-1,2-diol
1,2-Ethandiol
Ethylene glycol
Ethane-1,2-diol
1,2-Ethanediol
Ethane-1,2-diol
1,2-Ethanediol
Molmasse
AGW
Dichte
Schmelzpunkt
Siedepunkt
Wasserlöslichkeit
Brechungsindex
Explosionsgrenzen
Flammpunkt
Zündpunkt
AGW
Dichte
Schmelzpunkt
Siedepunkt
Wasserlöslichkeit
Brechungsindex
Explosionsgrenzen
Flammpunkt
Zündpunkt
62,068 g/mol
10 ml/m3 (TRGS 900)
1,1135 g/cm3
−13 °C
+197,5 °C
vollständig mischbar
1,4318 (bei 20 °C)
3,2 bis 22 Vol.-% (Luft)
+111 °C
+398 °C
10 ml/m3 (TRGS 900)
1,1135 g/cm3
−13 °C
+197,5 °C
vollständig mischbar
1,4318 (bei 20 °C)
3,2 bis 22 Vol.-% (Luft)
+111 °C
+398 °C
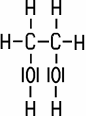
Klare, farblose und viskose Flüssigkeit

Frostschutzmittel mit Ethylenglycol müssen in der Garage in einem
verschlossenen Schrank unzugänglich für Kinder gelagert
werden. Sie dürfen nicht zusammen mit Lebensmittel aufbewahrt
werden. Am besten ist es, auf die Lagerung ganz zu verzichten.
Wirkung auf den menschlichen Körper
Die Aufnahme von Ethylenglycol führt zu Vergiftungserscheinungen. Nach Vergiftungen können Lungen-, Herz- und Nierenschäden auftreten. Zuerst entstehen Magen-Darm-Probleme mit Erbrechen und Durchfall. Hinzu kommen Schwindel, Atemnot oder Halluzinationen. Dann beschleunigt sich der Puls, Herzprobleme oder ein Lungenödem können entstehen. Bei höheren Dosen tritt schon in dieser Phase der Tod durch Herzversagen auf. Falls dies nicht passiert, werden nach ein bis drei Tagen die Nieren geschädigt. Nach etwa einer Woche treten schwere Schäden am Zentralnervensystem auf. Als mittlere, tödliche Dosis gelten etwa 1,4 Milliliter pro Kilogramm Körpergewicht. Die Dämpfe üben eine schwach reizende Wirkung auf Augen und Schleimhäute aus.
Chemisch-physikalische Eigenschaften
Ethylenglycol ist eine süßlich schmeckende, leicht zähflüssige Flüssigkeit. Sie vermischt sich sehr gut mit Wasser, sie ist aber auch in Aceton, Ethylalkohol und Diethylether gut löslich. Ein Gemisch mit je einem Anteil Wasser und Ethylenglycol gefriert erst unterhalb von −40 °C, daher eignen sich solche Gemische als Frostschutzmittel. Beim Siedepunkt beginnt sich Ethylengylcol zu zersetzen.
Ethylenglycol ist wie Glycerin stark hygroskopisch und zieht Feuchtigkeit aus der Luft an. Von Glycerin kann es so unterschieden werden:
I.) Iodprobe: Ethylenglycol löst Iod mit rotbrauner Farbe, Glycerin löst nur wenig Iod mit hellgelber Färbung.
II.) Gentianaviolettprobe: Ethylenglycol löst Gentianaviolett mit violetter Farbe, Glycerin löst den Farbstoff gar nicht.
Beim Erhitzen mit konzentrierter Schwefelsäure entsteht Dioxan, eine aromatisch riechende Flüssigkeit und bedeutendes Lösungsmittel in der chemischen Technik. Ethylenglycol gehört aufgrund der zwei OH-Gruppen zu den zweiwertigen Alkoholen. Es lässt sich stufenweise bis zur Oxalsäure oxidieren.
Die Aufnahme von Ethylenglycol führt zu Vergiftungserscheinungen. Nach Vergiftungen können Lungen-, Herz- und Nierenschäden auftreten. Zuerst entstehen Magen-Darm-Probleme mit Erbrechen und Durchfall. Hinzu kommen Schwindel, Atemnot oder Halluzinationen. Dann beschleunigt sich der Puls, Herzprobleme oder ein Lungenödem können entstehen. Bei höheren Dosen tritt schon in dieser Phase der Tod durch Herzversagen auf. Falls dies nicht passiert, werden nach ein bis drei Tagen die Nieren geschädigt. Nach etwa einer Woche treten schwere Schäden am Zentralnervensystem auf. Als mittlere, tödliche Dosis gelten etwa 1,4 Milliliter pro Kilogramm Körpergewicht. Die Dämpfe üben eine schwach reizende Wirkung auf Augen und Schleimhäute aus.
Chemisch-physikalische Eigenschaften
Ethylenglycol ist eine süßlich schmeckende, leicht zähflüssige Flüssigkeit. Sie vermischt sich sehr gut mit Wasser, sie ist aber auch in Aceton, Ethylalkohol und Diethylether gut löslich. Ein Gemisch mit je einem Anteil Wasser und Ethylenglycol gefriert erst unterhalb von −40 °C, daher eignen sich solche Gemische als Frostschutzmittel. Beim Siedepunkt beginnt sich Ethylengylcol zu zersetzen.
Ethylenglycol ist wie Glycerin stark hygroskopisch und zieht Feuchtigkeit aus der Luft an. Von Glycerin kann es so unterschieden werden:
I.) Iodprobe: Ethylenglycol löst Iod mit rotbrauner Farbe, Glycerin löst nur wenig Iod mit hellgelber Färbung.
II.) Gentianaviolettprobe: Ethylenglycol löst Gentianaviolett mit violetter Farbe, Glycerin löst den Farbstoff gar nicht.
Beim Erhitzen mit konzentrierter Schwefelsäure entsteht Dioxan, eine aromatisch riechende Flüssigkeit und bedeutendes Lösungsmittel in der chemischen Technik. Ethylenglycol gehört aufgrund der zwei OH-Gruppen zu den zweiwertigen Alkoholen. Es lässt sich stufenweise bis zur Oxalsäure oxidieren.
Ethylenglycol wird in der chemischen Industrie aus Ethylenoxid
und Wasser unter Druck hergestellt. Dabei
öffnet sich der Ring, und das Wasser-Molekül wird addiert:
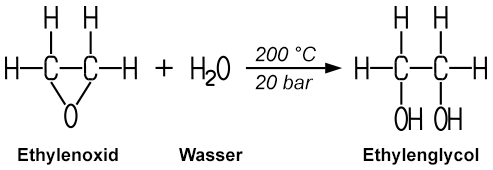
Verwendet man stark verdünnte Säuren, gelingt die Ringöffnung schon bei Zimmertemperatur. Eine andere Herstellungsmöglichkeit ist der Einsatz des OMEGA-Prozesses (Only Mono Ethylene Glycol Advanced Process): Mit Hilfe von Katalysatoren wird das Ethylenoxid mit Kohlenstoffdioxid zu Ethylencarbonat umgewandelt. Durch eine Hydrolyse dieses Zwischenproduktes gewinnt man dann das Ethylenglycol.
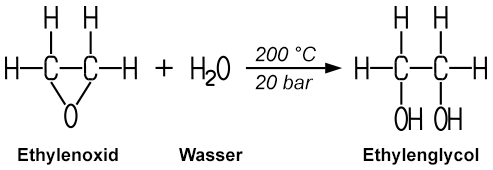
Verwendet man stark verdünnte Säuren, gelingt die Ringöffnung schon bei Zimmertemperatur. Eine andere Herstellungsmöglichkeit ist der Einsatz des OMEGA-Prozesses (Only Mono Ethylene Glycol Advanced Process): Mit Hilfe von Katalysatoren wird das Ethylenoxid mit Kohlenstoffdioxid zu Ethylencarbonat umgewandelt. Durch eine Hydrolyse dieses Zwischenproduktes gewinnt man dann das Ethylenglycol.
Ethylenglycol wird als Frostschutzmittel im
Kühlwasser von Kraftfahrzeugen und zur Enteisung von Flugzeugen
verwendet. Es dient als Kühl- und Schmiermittel bei
Hochleistungsmotoren. Gelegentlich wird es auch als Desinfektionsmittel
für große Räume eingesetzt. Ethylenglycol ist ein
wichtiges Zwischenprodukt zur Herstellung von Polyethylenterephthalat,
einem wichtigen Polyester. Es wird auch zur Herstellung des
Lösungsmittels Dioxan benötigt.
© Thomas Seilnacht / Benutzerhandbuch / Lizenzbestimmungen / Impressum / Datenschutz / Literaturquellen