|
|
|
Beim
Umkristallisieren löst man einen verunreinigten
Stoff in einem geeigneten, erwärmten Lösungsmittel und lässt
ihn dann beim Abkühlen wieder auskristallisieren. Die Kristallisation kann
durch das Zufügen eines kleinen Impfkristalls des beteiligten Stoffes
oder durch Kratzen mit einem Glasstab an der Schalen-Wand beschleunigt
werden.
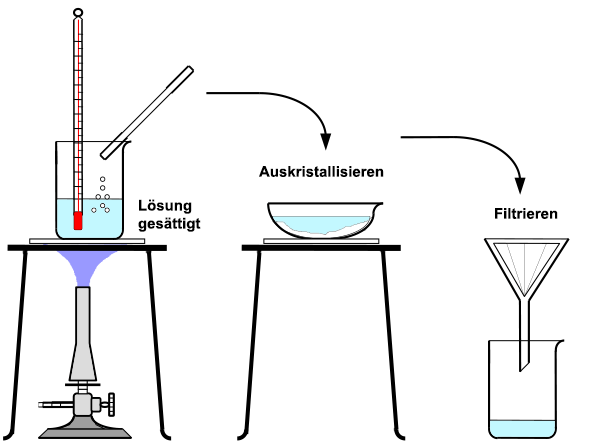
Umkristallisieren aus einer heißen, gesättigten Lösung Das ideale Lösungsmittel zum Umkristallisieren löst in der Kälte nur wenig und bei Wärme viel des Stoffes. Die Verunreinigungen verbleiben in der überstehenden Lösung. Sie können durch die Zugabe von Adsorptionsmitteln wie Aktivkohle aus der Lösung gezogen werden. Allerdings
darf das Lösungsmittel nicht vollständig verdampfen, sondern
es wird nach einer Weile durch Dekantieren oder
Filtrieren abgetrennt. Zur Herstellung eines
ganz reinen Stoffes wiederholt man den Vorgang des Umkristallisierens in
der Regel mehrfach. Die gereinigten Kristalle werden durch Trocknen
vom Lösungsmittel getrennt. Die Reinheit kann man dann durch eine
Schmelzpunktbestimmung abschätzen.
Salze, die sich in ihrer Löslichkeit stark unterscheiden, können in einer fraktionierten Kristallisation voneinander getrennt werden. Beim Abkühlen der Lösung scheidet sich dann zuerst das am schlechtesten lösliche Salz aus, so dass es von den übrigen noch gelösten Salzen abgetrennt werden kann. Beim Ausfällen wird eine unerwünschte Verunreinigung durch Zugabe eines geeigneten Reagenz ausgefällt. Das Ausfällen beruht auf einer chemischen Reaktion. Ist Wasser beispielsweise mit Chlorid-Ionen verunreinigt, fällt bei der Zugabe von Silbernitrat-Lösung schwer lösliches Silberchlorid AgCl aus, das durch Filtration leicht von der Lösung abgetrennt werden kann: AgNO3 +
KCl
Beim
Umfällen führt man einen schwer
löslichen Stoff durch chemische Reaktion mit einem anderen Stoff in
eine lösliche Verbindung über und fällt diese Verbindung
mit einem Fällungsmittel wieder aus. Beispiel: Die schwer lösliche
Benzoesäure wird mit Natriumhydroxidlösung
(Natronlauge) zu dem löslichen Natriumsalz Natriumbenzoat umgewandelt.
Die Verunreinigungen bleiben nach dem Filtrieren im Rückstand zurück.
Durch Neutralisation und durch Zugabe
von Salzsäure fällt die schwer
lösliche Benzoesäure wieder aus. Nach erneutem Filtrieren und
nachfolgendem Trocknen erhält man dann
die gereinigte Benzoesäure.
Benzoesäure (unlöslich)
+ NaOH
Natriumbenzoat (löslich) + HCl |