1235,86 g/mol (Tetrahydrat)
keine Angaben
2,498 g/cm3 (Tetrahydrat)
+90 °C (Tetrahydrat)
100g H2O lösen 40 g (L Tetrahydrat)
Farblose Kristalle oder weißes, kristallines Pulver
Ammoniummolybdat Tetrahydrat kommt als weißes, kristallines Pulver in den Handel. Es ist auch unter der Bezeichnung Ammoniumheptamolybdat bekannt. Das Tetrahydrat bildet klare, farblose oder leicht gelbgrüne Kristalle als sechsseitige Prismen. Beim Erhitzen auf über 90 °C geben die Kristalle ihr Kristallwasser ab. Das Salz löst sich gut im Wasser unter Bildung einer sauren Lösung.
Ammoniummolybdat verwittert an der Luft unter Freisetzung von Ammoniak. Aus diesem Grund ist der Stoff im Labor nur etwa ein bis zwei Jahre haltbar. In der Reagenz-Lösung zerfällt es ebenfalls, daher müssen alle Lösungen direkt vor dem Gebrauch mit unzersetztem Salz angesetzt werden. Mit
Phosphat-Ionen bildet Ammoniummolybdat nach vorangegangener Behandlung der Stoffprobe mit
Salpetersäure in wässriger Lösung einen gelben Niederschlag. Mit Säuren reagiert es unter Bildung der entsprechenden Ammoniumsalze und Molybdän(VI)-oxid. Mit
Ascorbinsäure entsteht in einer wässrigen Lösung nach dem vorsichtigen Erhitzen Molybdänblau. Diese Reaktion weist das Vorhandensein von
Molybdän-Ionen nach.

Beim Erhitzen einer wässrigen Ammoniummolybdat-Lösung mit Ascorbinsäure
entsteht zuerst eine Gelbfärbung, die allmählich in eine Blaufärbung übergeht.
Die Herstellung erfolgt durch Einwirkung von konzentrierter, heißer
Ammoniaklösung auf Molybdän(VI)-oxid. Gibt man zu Molybdän(VI)-oxid eine starke alkalische Lösung, so bilden sich Molybdat-Ionen:
MoO
3 + 2 OH
− 
MoO4
2− + H
2O
Durch eine Säurezugabe in der Molybdat-Lösung steigt die Protonenkonzentration, und es entsteht durch eine Zusammenlagerung ein Komplex, der aus sieben Molybdän-Atomen aufgebaut ist:
MoO
42− + 8 H
+ 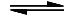
Mo
7O
246− + 4 H
2O
Im Labor wird Ammoniummolybdat als Nachweisreagenz für Phosphate eingesetzt. Es wird auch zum Nachweis von Kieselsäuren, Phosphorsäure, Arsen, Blei oder Sorbit benötigt. Die chemische Industrie braucht es zur Herstellung von
Katalysatoren.
Analytik
Ammoniummolybdat dient im analytischen Labor zum Nachweis von
Phosphaten. Auf eine Tüpfelplatte wird nur wenig der zu untersuchenden Substanz gegeben. Es kommen drei Tropfen 10%ige Salpetersäure hinzu und danach drei Tropfen gesättigte Ammoniummolybdat-Lösung. Das Auftreten eines gelben Niederschlags mit Ammoniummolybdophosphat weist auf Phosphat-Ionen hin:
PO
43− + 24 H
3O
+ + 3 NH
4+ + 12 MoO
42− 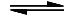
(NH
4)
3[P(Mo
3O
10)
4] ↓ + 36 H
2O
Zur Herstellung einer gesättigten Ammoniummolybdat-Lösung werden 40 g Ammoniummolybdat Tetrahydrat in 100 ml Wasser gelöst.
Didaktisches Material
Durchführung einer chemischen Analyse im
virtuellen Labor
Phosphate im Lexikon der Säuren, Basen und Salze


