Geschichte der Kalknutzung

Alter Kalkofen bei Marchtal
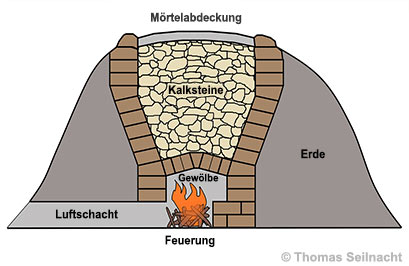
 Aufbau eines Kalkofens
Aufbau eines Kalkofens
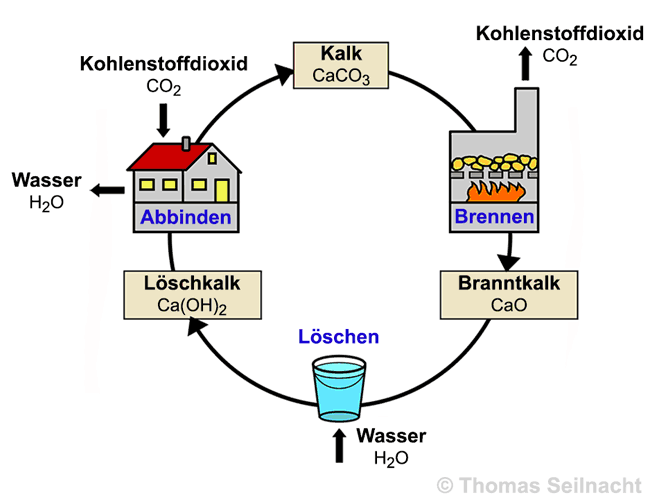
Kalk war früher das wichtigste Rohmaterial zur Herstellung von Mörtel. Gelöschter Kalk fand Verwendung als Düngemittel, zur Herstellung von Wandfarben oder als Frostschutzmittel für Obstbäume. Kalkmilch, eine wässrige Lösung von gelöschtem Kalk in Wasser, diente zur Bekämpfung von Schädlingen an Obstbäumen. Filtriert man die Kalkmilch, erhält man eine klare Lösung, die als Kalkwasser bezeichnet wird. Sie dient im chemischen Labor zum Nachweis von Kohlenstoffdioxid. Die Lösung trübt sich beim Durchleiten von Kohlenstoffdioxid weißlich.

Alter Kalkofen bei Marchtal
Kalkstein und Marmor
wurden schon in der Antike abgebaut und verarbeitet. Die 137 Meter hohe
Cheops-Pyramide ist aus über zwei Millionen mächtigen Kalksteinblöcken
gebaut. In der Bibel wurden die Begriffe „Kalkmörtel“ und „Kalktünche“ verwendet. Der griechische Philosoph Theophrast (geboren um 327 vor Christus)
berichtete über das Brennen von Kalk zu Branntkalk und über die
Herstellung von Kalkmörtel. Der lateinische Name calx taucht bei Gaius
Plinius dem Älteren (23–79 nach Christus) auf. Die Römer führten
den Kalk als Baustoff in Germanien ein und entwickelten die Kalkbrenntechnik
zu einem hohen industriellen Standard. In Deutschland kann in Bad Münstereifel eine römische Kalkbrennerei besichtigt werden.

Beim Kalkbrennen werden rohe, vom Steinbruch kommende Kalksteine auf 900 bis 1200 °C erhitzt. Der
Ofen ist innen mit Steinen aus Kalk gemauert und außen mit Erde umgeben,
damit der Ofen dem Druck des Füllmaterials standhält. Die zu
brennenden Kalksteine werden über dem Gewölbe vorsichtig aufeinander
geschichtet. Die Feuerung erfolgt durch ein Schürloch und dauert mindestens
100 Stunden. Bei diesem Vorgang entweicht Kohlenstoffdioxid, wobei Calciumoxid entsteht:
CaCO3  CaO + CO2
CaO + CO2
Man erhält einen
weißlichen, porösen Stoff,
der leicht zerbröckelt werden kann. Gibt man zu dem gebrannten
Kalk portionsweise Wasser, erhält
man gelöschten Kalk oder Calciumhydroxid.
Bei diesem Vorgang, der auch als „Kalklöschen“ bezeichnet wird,
wird Wärme frei, die so groß werden kann, dass die
Lösung zu sieden
beginnt. Als Produkt erhält man ein weißes, lockeres Pulver:
CaO + H2O  Ca(OH)2
Ca(OH)2
Gibt man Wasser im Überschuss
und die dreifache Menge Sand hinzu, erhält man Kalkbrei,
der als Mörtel geeignet ist. Beim Abbinden reagiert der Kalkbrei mit
dem Kohlenstoffdioxid der Luft und bildet wieder kristallinen, harten Kalk:
Kalk war früher das wichtigste Rohmaterial zur Herstellung von Mörtel. Gelöschter Kalk fand Verwendung als Düngemittel, zur Herstellung von Wandfarben oder als Frostschutzmittel für Obstbäume. Kalkmilch, eine wässrige Lösung von gelöschtem Kalk in Wasser, diente zur Bekämpfung von Schädlingen an Obstbäumen. Filtriert man die Kalkmilch, erhält man eine klare Lösung, die als Kalkwasser bezeichnet wird. Sie dient im chemischen Labor zum Nachweis von Kohlenstoffdioxid. Die Lösung trübt sich beim Durchleiten von Kohlenstoffdioxid weißlich.
| Kalk ist neben Ton Hauptbestandteil
des Rohmaterials zur Herstellung von Zement. |
Manche Zahnpasten oder
auch Putzmittel enthalten Kalk als sanftes Scheuermittel. |
Aufgrund der vielfältigen
Erscheinungsformen des Kalks wurde erst spät die „Grundsubstanz“ entdeckt.
Erasmus Bartholinus unternahm im Jahre 1669 physikalische Untersuchungen
am Kalkspat vor, und erst im Jahre 1804 führte Buchholz eine korrekte
chemische Analyse durch. Die Chemiker nennen diese Grundsubstanz heute
Calciumcarbonat, die Mineralogen Calcit und bei
veränderter Strukur Aragonit. Die Geologen oder die Petrographen
bezeichnen Steine, die aus dieser Grundsubstanz aufgebaut sind, als Kalkstein oder Marmor. Kalk
ist heute immer noch ein wichtiger Rohstoff und findet sich in zahlreichen
Produkten.
| Kalk verbessert die technischen Eigenschaften des PVCs. |
In der Grundmasse der
Radiergummis ist Kalkpulver als Scheuermittel enthalten. |
Weitere Materialien
Stoffe in der Chemikaliendatenbank: Calciumcarbonat, Calciumoxid, Calciumhydroxid
Kopiervorlage zum Kreislauf der Kalkverarbeitung
Serienbilder: Aufbau eines Kalkofens, Kreislauf der Kalkverarbeitung
Stoffe in der Chemikaliendatenbank: Calciumcarbonat, Calciumoxid, Calciumhydroxid
Kopiervorlage zum Kreislauf der Kalkverarbeitung
Serienbilder: Aufbau eines Kalkofens, Kreislauf der Kalkverarbeitung