 |
 Klare, farblose Flüssigkeit |
Molmasse 102,089 g/mol AGW 0,1 ml/m3 (TRGS 900) Dichte 1,082 g/cm3 Schmelzpunkt −73,4 °C Siedepunkt +139,5 °C Wasserlöslichkeit zersetzt sich Brechungsindex (20°C) 1,3901 Explosionsgrz. 2,7 bis 10,3 Vol.-% (Luft) Flammpunkt +49 °C Zündpunkt +316 °C |
| Piktogramme GHS 02 GHS 05 GHS 06 Gefahr |
Gefahrenklassen
+ Kategorie Entzündbare Flüssigkeiten 3 Akute Toxizität oral 4 Akute Toxizität inhalativ 3 Ätz-/Reizwirkung auf die Haut 1B Spez. Zielorgantoxizität 3 (Atemwege) |
HP-Sätze (siehe auch Hinweis) H 226, 302, 314, 331, 335 P 210, 260, 280.1-4+7, 312, 303+361+353, 305+351+338 Entsorgung Vorbehandlung erforderlich |
| Etikett drucken | Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
| CAS 108-24-7 | Essigsäureanhydrid Acetanhydrid |
Acetic anhydride |
Bemerkung
für Schulen: Essigsäureanhydrid reagiert mit Wasser, mit
Säuren und Laugen und mit Alkoholen. Die Vorschriften zur Entsorgung sind zu beachten. Die stechend riechende und tränenreizende Flüssigkeit wirkt toxisch beim Einatmen und verätzt Haut und Augen. Beim
Arbeiten müssen Schutzbrille, Schutzkittel, Schutzhandschuhe aus
Butylkautschuk und ein Gesichtsschild getragen werden. Das Arbeiten im
Abzug wird empfohlen. |
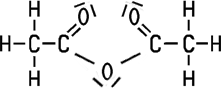
| Eigenschaften Essigsäureanhydrid
ist eine farblose, klare Flüssigkeit, die stark stechend riecht
und die Augen reizt. Bei der Zugabe von Wasser zersetzt sie sich zu Essigsäure,
bei der Alkoholzugabe entsteht ein Ester. Die Zersetzung im Wasser
erfolgt in heißem Wasser oder bei der Zugabe von Säuren
wesentlich schneller. Der Siedepunkt liegt höher als der von
Essigsäure.
 |
| Herstellung Essigsäureanhydrid entsteht, wenn zwei Moleküle Essigsäure unter Wasserabspaltung reagieren. Dabei verbinden sich die beiden
Carboxygruppen der Essigsäure. Damit dies gelingt, wird
Essigsäure zunächst unter Wasserabspaltung zu einem Keten
umgesetzt, das sich anschließend an die Essigsäure addiert.
Eine weitere industrielle Herstellungsmöglichkeit wäre die
Oxidation von Acetaldehyd am Kupferacetat-Kontakt. Im Labor kann man Essigsäureanhydrid durch die Reaktion von Acetylchlorid mit Natriumacetat erhalten: 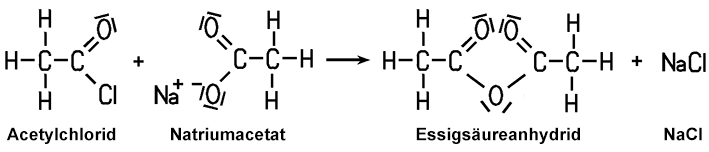 |
| Verwendung Essigsäureanhydrid
ist ein bedeutendes Acetylierungsmittel. Es wird zur Herstellung von
Celluloseacetat benötigt, das als Textilgewebe zahlreiche
Anwendungen findet, beispielsweise in Textilien oder in optischen
Schichten der Smartphone-Monitore. Bei der Herstellung des
schmerzstillenden Medikaments Acetylsalicylsäure, das unter dem Markennamen Aspirin bekannt ist, reagiert Salicylsäure
mit Essigsäureanhydrid. Der Handel mit Essigsäureanhydrid
wird überwacht, da es ein bedeutender Grundstoff zur Synthese von
Diacetylmorphin (Heroin) aus Morphin ist. |