| Inhalt Benennung Stoffbeispiele Herstellung Eigenschaften Verwendung | 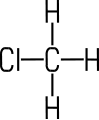 Chlormethan | Die
Halogenkohlenwasserstoffe als Stoffgruppe der organischen
Chemie enthalten im Grundgerüst einen Kohlenwasserstoff
und mindestens ein Halogen-Atom. Chlormethan ist ein einfacher Vertreter der Gruppe. |
Benennung der Halogenkohlenwasserstoffe
Die Moleküle der Halogenkohlenwasserstoffe enthalten ein Grundgerüst aus einem Kohlenwasserstoff, bei dem Wasserstoff-Atome durch Iod-, Brom-, Chlor- oder Fluor-Atome ersetzt sind. Sie sind vor allem durch die Fluorchlorkohlenwasserstoffe FCKW bekannt geworden. Diese gehören zu den Hauptverursachern des Ozonlochs. Aber auch einige andere Halogenkohlenwasserstoffe besitzen dieses Potenzial.
Nach der IUPAC-Nomenklatur
erfolgt die Benennung durch das Voransetzen der vorhandenen Halogen-Atome
vor dem Namen des Kohlenwasserstoff-Grundgerüstes. Sind mehrere Halogen-Atome in einem
Molekül enthalten, werden diese in alphabetischer Reihenfolge genannt. Bei den Fluorchlorkohlenwasserstoffen FCKW
ist auch die umgekehrte Reihenfolge üblich, weil sich das in der
Alltagssprache so eingebürgert hat. Bei der Summenformel werden
zuerst die C-, und die H-Atome aufgezählt, dann erst die
Halogen-Atome.
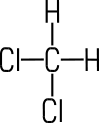
| Name IUPAC | Chlor- methan | Dichlor- methan |
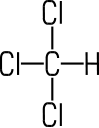
Trichlor- methan |
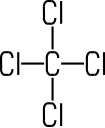
Tetrachlor- methan |
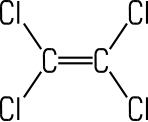
Tetrachlor- ethen |
| Struktur- formel |
 |
 |
 |
 |
 |
| Summen- formel |
CH3Cl | CH2Cl2 | CHCl3 | CCl4 | C2Cl4 |
| Trivialname | Methylchlorid | Methylenchlorid | Chloroform | Tetrachlorkohlenstoff | Per |
Beispiele für aliphatische Halogenkohlenwasserstoffe
Chlormethan (Methylchlorid)
Chlormethan ist ein farbloses, schwach
süßlich riechendes, giftiges Gas, das
narkotisierend wirkt.
Der Siedepunkt liegt bei −23,8 °C. Das Einatmen des Gases kann zu schweren Nervenschädigungen
führen. Leber-,
Nieren- und Herzversagen führen schließlich zum
Tode. Außerdem
steht es im Verdacht, eine krebserzeugende Wirkung zu
besitzen. Es wird
in der organischen Chemie als Zwischenprodukt zur Herstellung
von anderen
organischen Verbindungen benötigt. Chlormethan darf nicht
mit Alkali- oder Erdalkalimetallen in Berührung kommen, da hierbei
eine Explosion auftreten kann.
Dichlormethan (Methylenchlorid)
Dichlormethan
ist eine farblose, nicht
brennbare Flüssigkeit, die in Wasser schwer, in Alkohol
leicht löslich
ist. Der Siedepunkt liegt bei +40 °C. Die
Flüssigkeit verdampft bereits bei Raumtemperatur. Die Dämpfe
reizen die Augen, höhere
Konzentrationen führen
zu Rauschzuständen und Bewusstlosigkeit. Wie Chlormethan
steht es
im Verdacht, eine krebserzeugende Wirkung zu besitzen.
Es schädigt die Leber, das Blut und das zentrale Nervensystem. Nach neueren Untersuchungen kann es wie Tetrachlormethan die Ozonschicht zerstören.
Dichlormethan dient
als Lösungsmittel und Extraktionsmittel für
Öle, Coffein,
Harze, Wachse und ist in Fleckreinigungsmittel enthalten. Als
Begasungsmittel wird es wie Brommethan oder Dichlorethan in
Schiffscontainern zur Bekämpfung von Schädlingen eingesetzt.
Dies kann beim Öffnen eines solchen Containers, sofern er vorher
nicht intensiv belüftet wurde, bei den Werftarbeitern oder
LKW-Fahrern zu schweren Vergiftungen führen. Mit
Alkalimetallen oder mit Aluminium-Pulver reagiert Dichlormethan in einer
Explosion. Diese Reaktion hat schon mehrfach zu schweren Unfällen in Laboren geführt. Auch
die anderen Halogenalkane können mit Natrium oder Kalium explosiv
reagieren. Natrium darf zum Beispiel nicht zum Trocknen von
Halogenalkanen verwendet werden.
Trichlormethan (Chloroform)
Chloroform wurde früher als
Pflanzenschutzmittel und als Narkosemittel verwendet. Diese Anwendungen
sind heute verboten, da es Leberschäden verursacht und im Verdacht
steht, krebserzeugend zu wirken. Außerdem besaß das Narkosemittel
ein hohes Risiko: Viele Patienten starben an Herz- und Kreislaufversagen
während der Narkose. Im Labor wird die süßlich riechende,
farblose und nicht brennbare Flüssigkeit als Lösungsmittel verwendet.
Unter Lichteinfluss bildet sich Phosgen und Chlorwasserstoff, daher wird es
in braunen Flaschen aufbewahrt. Das käufliche Chloroform ist mit Ethanol stabilisiert, der mit dem entstehenden Phosgen reagiert und das Gas unschädlich
macht.
Tetrachlormethan (Tetrachlorkohlenstoff)
Das Halogenalkan Tetrachlorkohlenstoff ist eine farblose, nicht
brennbare Flüssigkeit, die in Wasser nur wenig, in Ethanol, Ether
oder Benzin gut löslich ist und fette Öle oder Harze gut löst.
Wie Chloroform ist es stark leberschädigend und gehört zu
den Stoffen mit einem möglichen krebserzeugenden Potenzial. Außerdem
ist es schädlich für Wasserorganismen und schädigt die Ozonschicht.
Tetrachlorkohlenstoff ist sehr reaktionsträge und wird von Säuren
und Laugen nicht angegriffen. Unter Licht- und Wärmeeinwirkung entsteht
besonders in Anwesenheit von Feuchtigkeit das Giftgas Phosgen.
Daher ist seine Anwendung als Feuerschutzmittel heute verboten. Gemische
mit Alkalimetallen wie Natrium und Kalium oder mit Aluminiumpulver können heftig
explodieren. Tetrachlorkohlenstoff darf aufgrund der möglichen Gefahren
nicht mehr als Lösungsmittel verwendet werden.
Tetrachlorethen (PER)
Das Halogenalken PER ist ebenfalls eine farblose
nicht brennbare Flüssigkeit und wird heute in chemischen Reinigungen
zur Textilreinigung eingesetzt. Es ist ein ausgezeichnetes Lösungsmittel
für tierische und pflanzliche Fette und Öle. Trotzdem ist seine
Verwendung sehr problematisch: Es wirkt wie die anderen Halogenkohlenwasserstoffe
leberschädigend und gehört zu den im Verdacht stehenden, krebserzeugenden
Stoffen. Problematisch sind eventuell vorhandene Rückstände in
Textilien aus der chemischen Reinigung. Kleidungsstücke aus der chemischen
Reinigung sollten daher vor dem Tragen gut ausgelüftet werden. Das
Auslüften darf nicht in Wohn- oder Schlafräumen erfolgen. Besser
ist jedoch der vollständige Verzicht auf das chemische Reinigen. Ein
Blick auf das Etikett beim Kauf genügt, um zu entscheiden, ob das
Kleidungsstück selbst gewaschen werden kann:

Enthält ein Molekül
zwei verschiedene Halogen-Atome, werden diese in der Reihe des Alphabets
genannt. Die vorangestellten Ziffern kennzeichnen die Stellung der Halogen-Atome:
| Name (IUPAC) | Bromtrifluor- methan |
Dichlordifluor methan |
2-Brom-2-chlor 1,1,1-trifluorethan |
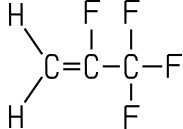
2,3,3,3-Tetra- fluorpropen |
| Struktur- formel |
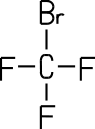 |
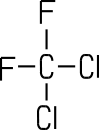 |
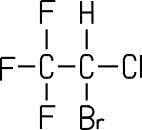 |
 |
| Trivialname | Halon 1301 | Frigen 12 |
Halothan | R-1234yf |
Bromtrifluormethan (Halon 1301)
Halon 1301 war früher aufgrund
seiner brandhemmenden Wirkung in Halon-Feuerlöschern enthalten. Die
Verwendung von Halonen in Feuerlöschern ist heute in Deutschland aufgrund der ozonschädigenden Wirkung nicht
mehr erlaubt. Als Halone werden alle brandhemmenden
Halogenkohlenwasserstoffe bezeichnet, zum Beispiel Tetrachlormethan (Halon 104),
Brommethan (Halon 1001) oder Bromchlordifluormethan (Halon 1211).
Dichlordifluormethan (Frigen 12)
Frigen 12 ist ein nicht
brennbares
Gas, das früher in großem Umfang in Kühlschränken
als komprimiertes Gas und als Treibgas in Spraydosen eingesetzt wurde.
Kohlenwasserstoffe
mit Chlor und Fluoratomen nennt man FCKW oder Fluorchlorkohlenwasserstoffe.
Diese Stoffe haben sich als Hauptverursacher für die Zerstörung
der lebensnotwendigen Ozonschicht in der Stratosphäre herausgestellt.
2-Brom-2-chlor-1,1,1-trifluorethan (Halothan)
Halothan ersetzt heute das früher
verwendete Chloroform als Narkosemittel. Es ist eine leicht flüchtige,
nicht brennbare Flüssigkeit mit einer Siedetemperatur von 50 °C.
Zur Narkose wird die Flüssigkeit verdampft und inhaliert. Bei wiederholten
Anwendungen kann es allerdings zu Leberschädigungen kommen.
2,3,3,3-Tetrafluorpropen (R-1234yf)
Das Halogenalken R-1234yf ist ein gasförmiges
Kältemittel für Kühlschränke und Klimaanlagen. Es greift
die Ozonschicht nicht an und zersetzt sich relativ schnell in der Atmosphäre.
Daher gilt es auch nicht als klimaschädigend. Allerdings entsteht
als Abbauprodukt die giftige Fluorverbindung Trifluoressigsäure. Beim
Einsatz in Klimaanlagen von Kraftfahrzeugen kann sich das Kältemittel
entzünden und Brände verursachen.
Herstellung der Halogenkohlenwasserstoffe
Halogenkohlenwasserstoffe kann man durch eine Substitutionsreaktion eines Alkans mit einem Halogen herstellen. Brom reagiert zum Beispiel mit Hexan, wenn dieses erwärmt und mit UV-Licht bestrahlt wird. Dabei entsteht Bromhexan und Bromwasserstoff HBr.
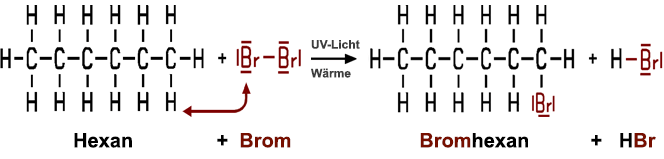
Eine andere Herstellungsmöglichkeit ist die Additionsreaktion eines Halogens an ein Alken oder an ein Alkin. Leitet man zum Beispiel Ethen in Brom oder in Bromwasser, verschwindet das Brom, ohne dass UV-Licht benötigt wird. Mit dieser Reaktion wird die Kohlenstoff-Mehrfachbindung nachgewiesen. Die Zweifachbindung im Ethen wird aufgebrochen, und zwei Brom-Atome addieren sich an das Molekül, so dass man als einziges Reaktionsprodukt 1,2-Dibromethan erhält.
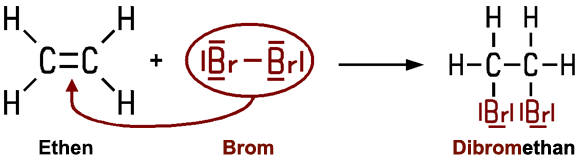
Eine weitere Herstellungsmöglichkeit der Halogenalkane ist die Additionsreaktion von Bromwasserstoff an ein Alken in der Gasphase oder in einem unpolaren Lösungsmittel:
HBr + Propen 1-Brompropan
1-Brompropan
Eigenschaften der Halogenkohlenwasserstoffe
Die meisten Halogenkohlenwasserstoffe haben ein gutes Lösungsvermögen für organische Lösungsmittel. Da die Kohlenstoff-Halogen-Bindung polar ist, besitzen die Halogenalkane einen höheren Siedepunkt als ein entsprechendes Alkan. Da sie nicht brennbar sind, wirken sie auch flammhemmend. Viele sind stark toxisch, schädigen die Leber oder können Krebs erzeugen. Einige wirken narkotisierend. FCKW's und einige andere zerstören die Ozonschicht.
Die Halogen-Atome in den Halogenkohlenwasserstoffen können dazu dienen, andere organische Stoffe herzustellen. Durch eine Eliminierungsreaktion kann man zum Beispiel aus 1,2-Dibromethan und Zinkpulver wieder Ethen herstellen. Wenn auch diese Reaktion technisch keine Bedeutung hat, weil Ethen auf anderem Weg viel günstiger hergestellt werden kann, wird sie oft im Chemieunterricht als Beispiel für eine typische Eliminierung herangezogen. Da 1,2-Dibromethan krebserzeugend ist, darf das Experiment an Schulen nicht mehr durchgeführt werden:
C2H4Br2 + Zn C2H4 + ZnBr2
C2H4 + ZnBr2
1,2-Dibromethan + Zink Ethen + Zinkbromid
Ethen + Zinkbromid
Die Halogen-Atome können auch durch eine Substitutionsreaktion ersetzt werden. Erhitzt man zum Beispiel Iodmethan mit Natriumhydroxid, erhält man Methanol und Natriumiodid. Das Iod-Atom wird durch eine Hydroxy-Gruppe ersetzt:
CH3I + Na+OH− CH3OH + Na+I−
CH3OH + Na+I−
Iodmethan + Natriumhydroxid Methanol + Natriumiodid
Methanol + Natriumiodid
Verwendung der Halogenkohlenwasserstoffe
Halogenkohlenwasserstoffe werden als Lösungsmittel, Treibmittel, Kühlmittel, Narkosemittel und auch zur Flammhemmung eingesetzt. Aufgrund ihres gefährlichen Potenzials ist der Einsatzbereich der meisten Stoffe für Experimente an Schulen stark eingeschränkt!
Insektizide wie DDT oder Lindan zählen ebenfalls zu den Halogenkohlenwasserstoffen. DDT ist ein aromatischer Halogenkohlenwasserstoff, Lindan ein cyclischer. Der Einsatz der beiden Stoffe ist heute in der EU und in der Schweiz verboten. DDT ist ein starkes Insektengift für Stechmücken und anderes Ungeziefer. Lindan wurde in Holzschutzmitteln, als Ameisengift oder zur Mottenbekämpfung eingesetzt. Es kann Säuglinge über die Muttermilch schädigen. Bei langanhaltender Aufnahme kleiner Mengen kann es zu chronischen Schäden am Zentralnervensystem kommen.
Herstellung der Halogenkohlenwasserstoffe
Halogenkohlenwasserstoffe kann man durch eine Substitutionsreaktion eines Alkans mit einem Halogen herstellen. Brom reagiert zum Beispiel mit Hexan, wenn dieses erwärmt und mit UV-Licht bestrahlt wird. Dabei entsteht Bromhexan und Bromwasserstoff HBr.

Beim Lösen von
Brom in Hexan entsteht eine gelbbraune Lösung. Diese Lösung wird mit
UV-Licht bestrahlt. Beim Belichten und beim Schütteln entfärbt sich die Lösung allmählich.
>Film
UV-Licht bestrahlt. Beim Belichten und beim Schütteln entfärbt sich die Lösung allmählich.
>Film
Eine andere Herstellungsmöglichkeit ist die Additionsreaktion eines Halogens an ein Alken oder an ein Alkin. Leitet man zum Beispiel Ethen in Brom oder in Bromwasser, verschwindet das Brom, ohne dass UV-Licht benötigt wird. Mit dieser Reaktion wird die Kohlenstoff-Mehrfachbindung nachgewiesen. Die Zweifachbindung im Ethen wird aufgebrochen, und zwei Brom-Atome addieren sich an das Molekül, so dass man als einziges Reaktionsprodukt 1,2-Dibromethan erhält.

Eine weitere Herstellungsmöglichkeit der Halogenalkane ist die Additionsreaktion von Bromwasserstoff an ein Alken in der Gasphase oder in einem unpolaren Lösungsmittel:
HBr + Propen
Eigenschaften der Halogenkohlenwasserstoffe
Die meisten Halogenkohlenwasserstoffe haben ein gutes Lösungsvermögen für organische Lösungsmittel. Da die Kohlenstoff-Halogen-Bindung polar ist, besitzen die Halogenalkane einen höheren Siedepunkt als ein entsprechendes Alkan. Da sie nicht brennbar sind, wirken sie auch flammhemmend. Viele sind stark toxisch, schädigen die Leber oder können Krebs erzeugen. Einige wirken narkotisierend. FCKW's und einige andere zerstören die Ozonschicht.
Die Halogen-Atome in den Halogenkohlenwasserstoffen können dazu dienen, andere organische Stoffe herzustellen. Durch eine Eliminierungsreaktion kann man zum Beispiel aus 1,2-Dibromethan und Zinkpulver wieder Ethen herstellen. Wenn auch diese Reaktion technisch keine Bedeutung hat, weil Ethen auf anderem Weg viel günstiger hergestellt werden kann, wird sie oft im Chemieunterricht als Beispiel für eine typische Eliminierung herangezogen. Da 1,2-Dibromethan krebserzeugend ist, darf das Experiment an Schulen nicht mehr durchgeführt werden:
C2H4Br2 + Zn
1,2-Dibromethan + Zink
Die Halogen-Atome können auch durch eine Substitutionsreaktion ersetzt werden. Erhitzt man zum Beispiel Iodmethan mit Natriumhydroxid, erhält man Methanol und Natriumiodid. Das Iod-Atom wird durch eine Hydroxy-Gruppe ersetzt:
CH3I + Na+OH−
Iodmethan + Natriumhydroxid
Verwendung der Halogenkohlenwasserstoffe
Halogenkohlenwasserstoffe werden als Lösungsmittel, Treibmittel, Kühlmittel, Narkosemittel und auch zur Flammhemmung eingesetzt. Aufgrund ihres gefährlichen Potenzials ist der Einsatzbereich der meisten Stoffe für Experimente an Schulen stark eingeschränkt!
| DDT | Lindan |
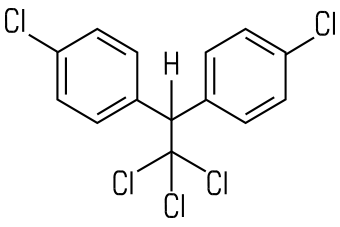 | 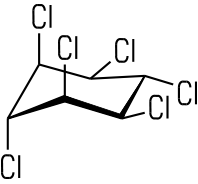 |
| Alte Bezeichnung: Dichlordiphenyltrichlorethan IUPAC: 1,1,1-Trichlor-2,2-bis(4-chlorphenyl)ethan | Alte Bezeichnung: Gammexan IUPAC: γ-Hexachlorcyclohexan |
Insektizide wie DDT oder Lindan zählen ebenfalls zu den Halogenkohlenwasserstoffen. DDT ist ein aromatischer Halogenkohlenwasserstoff, Lindan ein cyclischer. Der Einsatz der beiden Stoffe ist heute in der EU und in der Schweiz verboten. DDT ist ein starkes Insektengift für Stechmücken und anderes Ungeziefer. Lindan wurde in Holzschutzmitteln, als Ameisengift oder zur Mottenbekämpfung eingesetzt. Es kann Säuglinge über die Muttermilch schädigen. Bei langanhaltender Aufnahme kleiner Mengen kann es zu chronischen Schäden am Zentralnervensystem kommen.
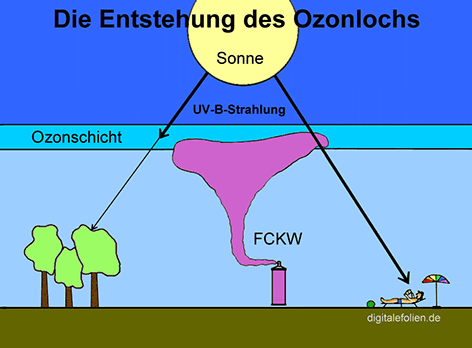
| Bedeutung der Grignard-Verbindungen | |||
|
Buch individuell erstellen: Basis-Text Halogenkohlenwasserstoffe


> Inhaltsverzeichnis