|
 Aussehen weißes, kristallines Pulver Vorkommen Pflanzen, Früchte, Trauben |
Molmasse 150,087 g/mol AGW 2 mg/m3 E (TRGS 900) Dichte 1,7598 g/cm3 Schmelzpunkt ca. +170 °C Wasserlöslichkeit Konz. bei 20 °C 1390 g/l (sauer) Flammpunkt +210 °C Zündpunkt +425 °C |
| Piktogramme GHS 05 Gefahr |
Gefahrenklassen
+ Kategorie Schwere Augenschädigung 1 |
HP-Sätze (siehe auch Hinweis) H 318 P 280.3, 305+351+338+310 Entsorgung G 3 |
| Etikett drucken | Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
| CAS 87-69-4 | L(+)-Weinsäure 2,3-Dihydroxybutandisäure 2,3-Dihydroxybernsteinsäure Threarsäure |
L-Tartaric acid 2,3-Dihydroxybutanedioic acid 2,3-Dihydroxysuccinic acid Racemic acid |
| Eigenschaften L(+)-Weinsäure bildet
farblose Kristalle nach dem monoklinen Kristallsystem. Das im Handel erhältliche kristalline Pulver erscheint weiß, es schmeckt stark sauer. Die Kristalle lösen sich sehr gut im Wasser. Sie sind auch in vielen Alkoholen gut löslich.
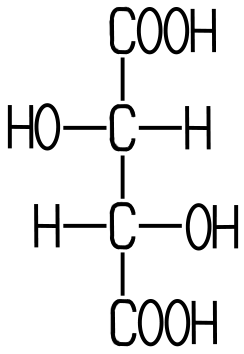
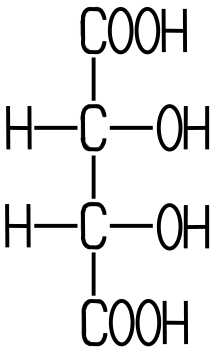
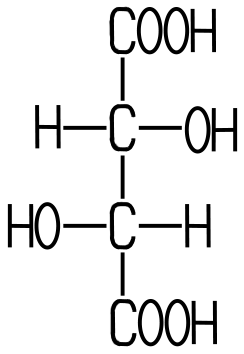
 Diese (teilweise zerbrochenen) Weinsäurekristalle sind etwa 0,5mm groß. Weinsäure ist eine relativ starke organische Säure. In der Natur kommt überwiegend die L(+)-Weinsäure vor. Es existieren zwei Enantiomere mit Spiegelbild-Isomerie: die L(+)-Weinsäure und die D(-)-Weinsäure. Die Meso-Weinsäure ist nur ein Diastereomer, weil sie sich nicht wie ein Spiegelbild zu den beiden anderen verhält.
Das Racemat, das Gemisch aus L(+)-Weinsäure
und D(-)-Weinsäure wird als Traubensäure bezeichnet. Es kommt wie die Meso-Weinsäure in der Natur nicht
vor, kann aber künstlich hergestellt werden.
Traubensäure aus einem alten Chemikalienbestand Beim vorsichtigen
Erhitzen
von L(+)-Weinsäure bilden sich Anhydride. Bei weiterem Erhitzen
tritt
unter Karamelgeruch Verkohlung ein. Die Salze der Weinsäure werden
Tartrate genannt. Ist nur ein Wasserstoff-Atom einer Carboxy-Gruppe
durch ein Metall-Atom
ersetzt, handelt es sich um Hydrogentartrate. Kaliumnatriumtartrat wird als Zusatzstoff in Lebensmitteln eingesetzt und ist
Bestandteil der Fehlingschen Lösung. Kaliumhydrogentartat wird im Backpulver verwendet. Weinstein ist ein Gemisch aus Kaliumhydrogentartrat und Calciumtartrat. Bei der Lagerung von Wein oder Traubensaft kann sich am Boden einer Fasses oder einer Flasche Weinstein bilden:
|
| Herstellung Zur Gewinnung von Weinsäure
wird Kaliumhydrogentartrat mit Calciumhydroxid zu Calciumtartrat umgewandelt. Bei der Zugabe von Schwefelsäure erhält man dann die Weinsäure. Ein ähnliches Verfahren wandte
der schwedische Chemiker Carl Wilhelm
Scheele (1742–1786) bei seiner Entdeckung der Weinsäure schon
im Jahr 1770 an. Weinstein kann aus dem Saft von Weintrauben gewonnen werden.
Er scheidet sich an den Wänden von Weinfässern ab. |
| Verwendung Weinsäure ist
als Lebensmittelzusatzstoff E 334 zugelassen, sie wird als
Komplexbildner, Säuerungsmittel
und Säureregulator verwendet. Sie dient auch zur Zubereitung von
Speiseeis,
Backpulver, Brausepulver, Kunsthonig, Limonaden und zur Säuerung
von
Wein. Weinsäure eignet sich als schonender Entkalker für
Kaffeemaschinen. Die Textilindustrie benötigt sie als
Reduktionsmittel beim Färben
und Drucken.
Komponenten eines Brausepulvers |