Neodym-Eisen-Bor-Legierungen wie Nd2Fe14B stellen Werkstoffe mit hohen ferromagnetischen Eigenschaften dar. Daraus lassen sich sehr starke
Magnete fertigen. Diese sind so stark, dass der Umgang mit
ihnen besondere Sicherheitsvorkehrungen benötigt. Sie können
Quetschwunden verursachen oder elektronische Geräte zerstören.
Bringt man einen solchen Magneten in die Nähe einer Armbanduhr,
werden Zeiger aus Stahl abgerissen. Neodym ist ein bedeutender Rohstoff für die Zukunft. Die Magnete werden zum Beispiel für Festplatten, aber auch für sehr leistungsfähige Elektrofahrzeuge benötigt.
| Schwebendes Graphit-Plättchen |

|
| Der Graphit ist diamagnetisch und wird von den Neodym-Supermagneten abgestoßen. |
Super-Magnete sind sehr starke Magnete, die unter anderem Neodym enthalten. Sie können
diamagnetische Materialien von paramagnetischen Materialien
unterscheiden. Dadurch können zum Beispiel ein gefälschter Goldbarren
oder eine falsche Goldmünze entlarvt werden: Eine an einem langen Faden hängende Münze aus Gold ist diamagnetisch und wird vom Super-Magneten leicht abgestoßen, während das paramagnetische Wolfram
leicht angezogen wird. Die gefälschten Goldbarren oder Münzen
enthalten Wolfram-Stäbe, die die gleiche Dichte wie Gold
aufweisen. Da die paramagnetische Wirkung allgemein viel stärker
als die diamagnetische ist, kann schon wenig Wolfram im Gold die
diamagnetische, abstoßende Wirkung am Super-Magnet aufheben. Silber ist ebenfalls diamagnetisch und wird vom Super-Magneten abgestoßen. Lit [120]
Neodym wird zur Erhöhung der mechanischen Eigenschaften mit anderen
Metallen legiert, zum Beispiel in Magnesiumlegierungen für den Flugzeugbau. Wie Cer dient es aufgrund seiner pyrophoren Eigenschaften zur Herstellung von
Feuersteinen. Neodym ist ein wichtiger Rohstoff zur Herstellung von
Aktivatoren für
Farbbildröhren. Es ist auch ein Bestandteil des
Nd-YAG-Lasers (Neodym-Yttrium-Aluminium-Granat-Laser). Neodym(III)-oxid-Zusätze färben Gläser rot bis violett. Diese Gläser werden in der Astronomie zum Kalibrieren eingesetzt.
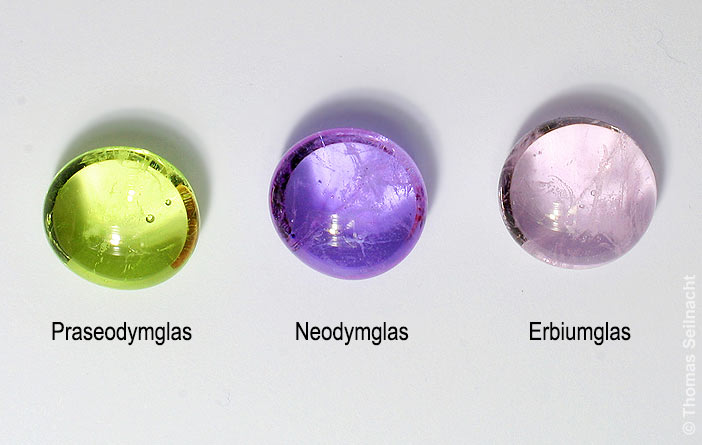
| Glasperlen mit Oxiden der Lanthaniden |
|
| Geringe Zugaben der Oxide zur Schmelze erzeugen farbige Gläser. |
|