 |
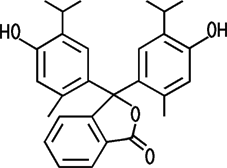 Weißes, kristallines Pulver |
Molmasse 430,536 g/mol AGW keine Angaben Dichte keine Angaben Schmelzpunkt +253 °C Wasserlöslichkeit kaum löslich |
| - |
- |
HP-Sätze H 280.1-3,5 Entsorgung G 3 |
| Etikett drucken | Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
| CAS 125-20-2 | Thymolphthalein 3,3-Bis(4-hydroxy-5-isopropyl-2-methylphenyl)-1(3H)-isobenzofuranon |
Thymolphthaleine 3,3-Bis(4-hydroxy-5-isopropyl-2-methylphenyl)-1(3H)-isobenzofuranone |
Bemerkung
für Schulen: Der Indikator Thymolphthalein kann als Ersatz für das krebserzeugende Phenolphthalein eingesetzt werden. Das Tragen einer Schutzbrille ist notwendig, beim
Freiwerden von Stäuben müssen auch Schutzhandschuhe und
Feinstaubmaske getragen werden.
Eigenschaften Thymolphthalein ist ein weißes, kristallines Pulver, das sich in Wasser kaum, in Ethanol, Aceton und alkalischen Lösungen gut löst. Der Indikator Thymolphthalein ist eine schwache Säure. Die 0,1%ige Lösung in Ethanol eignet sich als Indikatorlösung zum Bestimmen alkalischer Lösungen. Die neutrale Lösung ist farblos. Oberhalb von pH=9,3 schlägt die farblose Lösung nach blau um, bei stark alkalischen Lösungen um pH=14 tritt wieder eine Entfärbung auf. 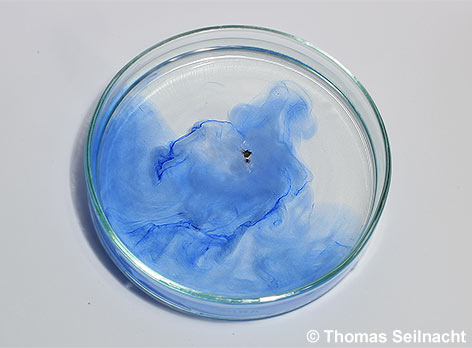 Bei der Reaktion von Lithium mit Wasser entsteht Wasserstoff und Lithiumhydroxid. Das Wasser wurde zuvor mit einer ethanolischen Thymolphthaleinlösung versetzt. |
| Herstellung Thymolphthalein
kann
durch das Erhitzen von Phthalsäureanhydrid mit
Thymol auf etwa
100 °C unter Zugabe von Zinn(IV)-chlorid
dargestellt werden. Nimmt man Phenol statt Thymol, entsteht in einer
vergleichbaren Reaktion Phenolphthalein. |
| Verwendung Im Labor wird Thymolphthalein als Säure-Base-Indikator vor allem beim Tritrieren alkalischer Lösungen verwendet. Von Bedeutung ist die Bestimmung des zweiten Äquivalenzpunktes der Phosphorsäure bei pH=9,7. Die ethanolische Lösung wird im Schullabor als Ersatz für Phenolphthalein eingesetzt. |