Das Wasser ist ein
wesentlicher
Stoff für das Leben auf der Erde. Es bedeckt zu mehr als zwei
Drittel
die Erdoberfläche. Auf der Erde kommen mehrere „Gestaltformen“ des
Wassers vor: Die Sonne verdunstet das Wasser zu Wasserdampf, als Regen
kommt es wieder auf die Erde zurück. Bei niedrigen Temperaturen im
Winter gefriert das Wasser zu Eis. Die Gletscher erinnern noch an die
Eiszeit, als ganz Mitteleuropa mit Gletschereis
überzogen war.
Bei heißen Quellen
wird das Wasser durch die Erdwärme erhitzt. In einem Geysir entsteht
am Fuß in einer trichterförmigen Erdhöhlung gasförmiges
Wasser, das durch seine plötzliche Ausdehnung beim Siedepunkt das
darüber stehende heiße Wasser in die Höhe schleudert. Dadurch
schießt heißer Wasserdampf in die Höhe. Wir kennen aus unserem
Alltag drei „Zustandsformen“ des Wassers. Eis ist der feste Zustand und
das Wasser der flüssige. Den gasförmigen Zustand des Wassers
sieht man an einem Teekessel als den unsichtbaren Teil zwischen der Austrittsstelle
und dort wo der Dampf sichtbar wird.
Die drei Zustandsformen nennt man auch Aggregatzustände. Wenn Wasser zu Sieden beginnt, verdampft Wasser zu Wasserdampf. Beim starken Abkühlen gefriert flüssiges Wasser zu festem Eis. Der Fachbegriff lautet hierzu erstarren. Den umgekehrten Vorgang, wenn sich Eis wieder verflüssigt, nennt man schmelzen. Kommt Wasserdampf mit einer kalten Glasscheibe in Berührung, kondensiert der Dampf wieder zu Wasser. Erhitzt man Wasser auf den Siedepunkt, beginnt es bei 100 °C zu sieden. Eis schmilzt am Schmelzpunkt bei 0 °C. Der Schmelzpunkt bei einem Stoff entspricht dem Erstarrungspunkt. Der Siedepunkt entspricht dem Kondensationspunkt.
Die drei Zustandsformen nennt man auch Aggregatzustände. Wenn Wasser zu Sieden beginnt, verdampft Wasser zu Wasserdampf. Beim starken Abkühlen gefriert flüssiges Wasser zu festem Eis. Der Fachbegriff lautet hierzu erstarren. Den umgekehrten Vorgang, wenn sich Eis wieder verflüssigt, nennt man schmelzen. Kommt Wasserdampf mit einer kalten Glasscheibe in Berührung, kondensiert der Dampf wieder zu Wasser. Erhitzt man Wasser auf den Siedepunkt, beginnt es bei 100 °C zu sieden. Eis schmilzt am Schmelzpunkt bei 0 °C. Der Schmelzpunkt bei einem Stoff entspricht dem Erstarrungspunkt. Der Siedepunkt entspricht dem Kondensationspunkt.
Im Haushalt begegnet
uns das Phänomen der Aggregatzustände überall. Beim Kochen
lässt man Fett oder Butter schmelzen. Schokolade schmilzt bereits
bei Sonneneinstrahlung. Beim Löten schmilzt man mit einem Lötkolben
das elektrisch leitfähige Lötzinn und verbindet so elektrische
Kontakte. Beim Zinngießen an Silvester muss das Zinn
auf seinen Schmelzpunkt von +232 °C erhitzt werden. Flüssiger Stickstoff wird zur Zubereitung von Speiseeis verwendet. Beim Umschütten verdampft er durch die Wärme im Raum, sein Siedepunkt liegt bei ungefähr −196 °C.
|
|
Hängt man nasse
Wäsche an eine Leine, dann trocknet die Wäsche allmählich.
Dieses Phänomen nennt man Verdunsten.
Hierbei geht das flüssige Wasser in den gasförmigen Zustand über,
ohne dass es auf seinen Siedepunkt erhitzt wird. Eine große Menge
an Wasser verdunstet auch über feuchten Böden, über Flüssen,
Seen und den Ozeanen.
Eine weitere Besonderheit
zeigen Stoffe, die beim Erhitzen des festen Zustandes direkt in den gasförmigen
Zustand übergehen. Das Phänomen wird als Sublimation bezeichnet. Gefrorenes Kohlenstoffdioxid oder Trockeneis sublimiert beispielsweise
bei −78,5 °C zu gasförmigem Kohlenstoffdioxid. Kohlenstoffdioxid
bildet unter Normaldruck keine Flüssigkeit, daher erhielt das tiefkalte
Kohlenstoffdioxid den Namen „Trockeneis“. Beim Abkühlen unter den Sublimationspunkt von −78,5 °C resublimiert
das Kohlenstoffdioxidgas wieder zu Trockeneis. Festes Iod geht beim Erhitzen direkt in gasförmigen Ioddampf über. Beim
Abkühlen von Ioddampf bilden sich durch Resublimation wieder Iodkristalle.
 |
Alltagssprache versus exakte Fachsprache der Chemie
Die Alltagssprache ist oft nicht exakt oder sie verwendet Begriffe als Synonyme, die so eigentlich gar nicht verwendet werden dürften. Betrachtet man kochendes Wasser von oben, ist der eigentliche Dampf unsichtbar. So wird umgangsprachlich sehr heißer Wassernebel und gasförmiges Wasser gleichgesetzt, beides wird dann unter Umständen „Wasserdampf“ genannt. Nach der chemischen Fachsprache entsteht beim Erhitzen und Verdampfen von Wasser im Teekessel ein Gas oder Dampf. Das, was man aber beim Teekessel am Dampfaustritt sieht, ist genaugenommen kein Dampf, sondern der Nebel, der durch das Abkühlen des Dampfs an der Luft entsteht. Der eigentliche Wasserdampf ist unsichtbar. Wir spüren vor allem die Hitze, wenn wir uns am Dampf verbrühen.
Die Alltagssprache ist oft nicht exakt oder sie verwendet Begriffe als Synonyme, die so eigentlich gar nicht verwendet werden dürften. Betrachtet man kochendes Wasser von oben, ist der eigentliche Dampf unsichtbar. So wird umgangsprachlich sehr heißer Wassernebel und gasförmiges Wasser gleichgesetzt, beides wird dann unter Umständen „Wasserdampf“ genannt. Nach der chemischen Fachsprache entsteht beim Erhitzen und Verdampfen von Wasser im Teekessel ein Gas oder Dampf. Das, was man aber beim Teekessel am Dampfaustritt sieht, ist genaugenommen kein Dampf, sondern der Nebel, der durch das Abkühlen des Dampfs an der Luft entsteht. Der eigentliche Wasserdampf ist unsichtbar. Wir spüren vor allem die Hitze, wenn wir uns am Dampf verbrühen.
Werden Wassertröpfchen in der Luft ganz fein verteilt, dann erhält man Nebel. In der Natur entsteht Nebel, wenn sich feuchte Luft abkühlt. Durch die Abkühlung kann die Luft nicht mehr so viel Feuchtigkeit aufnehmen, so dass das überschüssige Wasser in winzigen Tröpfchen kondensiert.
Nebel entsteht vorzugsweise im Winter an Gewässern. Die Sonne verdampft
tagsüber Wasser, am Abend kühlt es so stark ab, dass das Wasser
auskondensiert.
Die Bildung von Nebel
wird noch beschleunigt, wenn Kondensationskerne wie Rußpartikel vorhanden
sind. Wenn unterkühlter Wasserdampf bei Temperaturen unterhalb von
0 °C an Pflanzen oder am Boden direkt aus dem gasförmigen Zustand
in den festen Zustand übergeht, bildet sich Reif.
Daraus können bizarre Formen und Figuren an den Pflanzen und den Gegenständen
im Freien entstehen.
Im Chemieunterricht gelten
die drei Aggregatzustände fest, flüssig und gasförmig als
die drei klassischen Aggregatzustände.
Der feste Zustand eines Stoffes ist dadurch gekennzeichnet, dass eine Stoffportion
ihre Form behält. Eine Goldmünze bleibt im Gravitationsfeld der
Erde und im Bereich der Schwerelosigkeit in ihrer Form. Im flüssigen
Zustand füllen die flüssigen Stoffportionen auf der Erde die
Form eines Behälters aus und bilden oben eine ebene Oberfläche,
solange sie ruhen. Beim Herunterfallen wird eine Tropfenform gebildet.
Im Bereich der Schwerelosigkeit bilden Flüssigkeiten tendenziell Kugeln
aus. Gase haben in der Schwerelosigkeit hingegen die Tendenz, sich in alle
Richtungen auszubreiten. Im Schwerefeld der Erde können Gase Schichtungen
bilden. Ihre Tendenz, sich auszubreiten, ist auch im Schwerefeld gegeben.
Auf Druckerhöhung reagieren Flüssigkeiten und feste Stoffe kaum
mit Volumenminderung, solange sie in ihrem Aggregatzustand verbleiben.
Ändern sie ihren Aggregatzustand, können sie auch ihre Volumina
sprunghaft ändern. Gase dehnen sich bei Druckminderung aus, bei Druckerhöhung
sind verschiedene Möglichkeiten gegeben. Welche davon eintritt, kann
man am Zustandsdiagramm ablesen.
Beim Wasser besteht eine sogenannte „Anomalie“: Bei 4 °C besitzt Wasser die höchste Dichte. Beim Abkühlen unter diesen Temperaturwert dehnt sich das Wasser aus. Eis hat eine geringere Dichte als Wasser und schwimmt daher auf dem Wasser. Im Winter gefrieren aufgrund der Anomalie des Wassers die Gewässer nicht vollständig zu. Das dichtere und 4 °C warme Wasser sinkt auf den Boden. Wenn das Wasser an der Wasseroberfläche 0 °C erreicht, wird es fest und schwimmt auf dem Wasser. An einer Zirkulation kann dieses Wasser nicht mehr teilnehmen. Es isoliert sogar die unteren Wasserschichten gegen zu schnelle Abkühlung. Aus diesem Grunde können Wasserorganismen wie Fische im Winter im zugefrorenen See überleben. Das Phänomen der Ausdehnung von Flüssigkeiten beim Erstarren kommt nur bei wenigen anderen Stoffen vor.
Beim Wasser besteht eine sogenannte „Anomalie“: Bei 4 °C besitzt Wasser die höchste Dichte. Beim Abkühlen unter diesen Temperaturwert dehnt sich das Wasser aus. Eis hat eine geringere Dichte als Wasser und schwimmt daher auf dem Wasser. Im Winter gefrieren aufgrund der Anomalie des Wassers die Gewässer nicht vollständig zu. Das dichtere und 4 °C warme Wasser sinkt auf den Boden. Wenn das Wasser an der Wasseroberfläche 0 °C erreicht, wird es fest und schwimmt auf dem Wasser. An einer Zirkulation kann dieses Wasser nicht mehr teilnehmen. Es isoliert sogar die unteren Wasserschichten gegen zu schnelle Abkühlung. Aus diesem Grunde können Wasserorganismen wie Fische im Winter im zugefrorenen See überleben. Das Phänomen der Ausdehnung von Flüssigkeiten beim Erstarren kommt nur bei wenigen anderen Stoffen vor.
| Temperatur | Dichte |
| 0 °C (Eis) | 0,9168 g/ml |
| 0 °C (Wasser) | 0,999818 g/ml |
| 4 °C (Wasser) | 1,000000 g/ml |
| 10 °C (Wasser) | 0,999727 g/ml |
| 20 °C (Wasser) | 0,998231 g/ml |
Der Effekt, dass mit
Wasser gefüllte Spalten im Gebirge im Winter ganze Felswände
„sprengen“ können und das Phänomen der Frostschäden im Straßenbau
beruhen auf einem anderen Effekt: Kleine Kristalle sublimieren leichter
als größere Kristalle, und umgekehrt resublimieren Gase an großen
Kristallen besser als an kleinen. Bei längeren Frostperioden werden
daher die kleinen Kristalle immer kleiner und die größeren Kristalle
immer größer. Die größeren Kristalle entwickeln bei
ihrem Wachstum sehr beachtliche Kräfte, so dass große Felsen
abgesprengt oder faustgroße Beulen auf dem Straßenbelag entstehen
können.
Beim Siedepunkt geht eine Flüssigkeit in den gasförmigen Zustand über, die flüssige und die gasförmige Phase stehen dann in einem thermodynamischen Gleichgewichtszustand. Da der Siedepunkt vom Außendruck abhängig ist, gelten die tabellarischen Werte für den Siedepunkt eines Stoffes bei einem Normaldruck von 1013 mbar. Beim Erreichen des Siedepunktes unter Normalbedingungen entspricht der Dampfdruck einer Flüssigkeit dem äußeren Druck von 1013 mbar. Nach dieser Definition verdampft das Wasser nicht erst beim Siedepunkt von exakt 100 °C, sondern teilweise schon bei niedrigeren Temperaturen. Am Siedepunkt ist nur der beschriebene Gleichgewichtszustand erreicht.
Beim Erwärmen einer Flüssigkeit wird die zugeführte Wärme zunächst zum Aufheizen der Flüssigkeit verwendet. Je mehr sich die Temperatur der Flüssigkeit dem Siedepunkt nähert, umso mehr wird die Wärme zum Verdampfen der Flüssigkeit verbraucht. Beim Erreichen des Siedepunktes steigt die Temperatur für längere Zeit nicht mehr an, sie bleibt konstant. Die zugeführte Wärme dient dann nur noch dem Verdampfen der Flüssigkeit. An der konstant bleibenden Temperatur erkennt man das Erreichen des Siedepunktes. So lassen sich Stoffe an ihren Siedepunkten (oder auch an ihrem Schmelzpunkt) erkennen (>Siedepunktbestimmung). Bei der Destillation nutzt man den Siedepunkt zum Trennen von Stoffgemischen.
Beim Siedepunkt geht eine Flüssigkeit in den gasförmigen Zustand über, die flüssige und die gasförmige Phase stehen dann in einem thermodynamischen Gleichgewichtszustand. Da der Siedepunkt vom Außendruck abhängig ist, gelten die tabellarischen Werte für den Siedepunkt eines Stoffes bei einem Normaldruck von 1013 mbar. Beim Erreichen des Siedepunktes unter Normalbedingungen entspricht der Dampfdruck einer Flüssigkeit dem äußeren Druck von 1013 mbar. Nach dieser Definition verdampft das Wasser nicht erst beim Siedepunkt von exakt 100 °C, sondern teilweise schon bei niedrigeren Temperaturen. Am Siedepunkt ist nur der beschriebene Gleichgewichtszustand erreicht.
Beim Erwärmen einer Flüssigkeit wird die zugeführte Wärme zunächst zum Aufheizen der Flüssigkeit verwendet. Je mehr sich die Temperatur der Flüssigkeit dem Siedepunkt nähert, umso mehr wird die Wärme zum Verdampfen der Flüssigkeit verbraucht. Beim Erreichen des Siedepunktes steigt die Temperatur für längere Zeit nicht mehr an, sie bleibt konstant. Die zugeführte Wärme dient dann nur noch dem Verdampfen der Flüssigkeit. An der konstant bleibenden Temperatur erkennt man das Erreichen des Siedepunktes. So lassen sich Stoffe an ihren Siedepunkten (oder auch an ihrem Schmelzpunkt) erkennen (>Siedepunktbestimmung). Bei der Destillation nutzt man den Siedepunkt zum Trennen von Stoffgemischen.
Der Siedepunkt einer Flüssigkeit sinkt mit abnehmendem Druck und daher auch bei zunehmender Höhenlage. Pro 300 Höhenmeter sinkt der Siedepunkt um 1 °C. Wenn zum Beispiel auf dem Mount Everest bei fast 9000 Höhenmetern ein Druck von 312 mbar vorherrscht, dann liegt der Siedepunkt von Wasser nur noch etwa bei 70 °C. Aufgrund der Druckabhängigkeit werden Destillationen auch unter Vakuum durchgeführt. Die Abnahme des Drucks erniedrigt die Siedetemperatur, so dass weniger Energie beim Heizen aufgewendet werden muss.
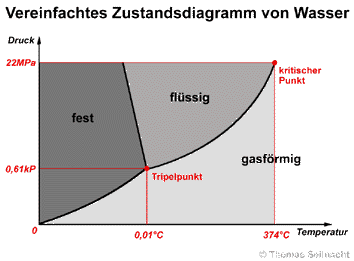
Setzt man den Außendruck (p) und die Temperatur (T) in ein Diagramm, lässt sich für ein Stoff ein sogenanntes Zustandsdiagramm (oder pT-Phasendiagramm) darstellen. Anhand der Linien erkennt man, bei welchem Druck und bei welcher Temperatur der Stoff seinen Zustand verändertSetzt man den Außendruck (p) und die Temperatur (T) in ein Diagramm, lässt sich für ein Stoff ein sogenanntes Zustandsdiagramm (oder pT-Phasendiagramm) darstellen. Anhand der Linien erkennt man, bei welchem Druck und bei welcher Temperatur der Stoff seinen Zustand verändert.
Auf den Linien selbst
liegt der thermodynamische Gleichgewichtszustand vor. Am Tripelpunkt
können alle drei Aggregatzustände gleichzeitig vorliegen. Unterhalb
des Tripelpunktes tritt das Phänomen der Sublimation auf, die Trennlinie
zwischen absolutem Nullpunkt und Tripelpunkt heißt Sublimationskurve.
Die Trennlinie zwischen fester und flüssiger Phase nennt man Schmelzkurve,
die Trennlinie zwischen flüssiger und gasförmiger Phase Siedekurve.
Beim kritischen Punkt können Gas und
Flüssigkeit aufgrund ihrer identischen Dichte nicht mehr unterschieden
werden. Man könnte sagen: Der Stoff ist sowohl gasförmig als
auch flüssig. Techniker in einem Kraftwerk, die mit Wasser am kritischen
Punkt arbeiten, sprechen von „überkritischem
Wasser“. Es lässt sich oberhalb des kritischen Punktes keine
Phasengrenzlinie mehr angeben.
Ergänzende Hinweise: Die Schmelzkurve beim Wasser unterscheidet sich von anderen Stoffen. Beim Schmelzen von Eis beobachtet man bei steigendem Druck ein Absinken des Schmelzpunktes. Dieses Phänomen nennt man Schmelzanomalie des Wassers. Das obige Zustandsdiagramm ist aus didaktischen und anschaulichen Gründen vereinfacht, außerdem sind im Diagramm die Proportionen nicht korrekt dargestellt. Bei sehr hohem Druck (nicht im Diagramm dargestellt) bildet das Eis eine weitere Zustandsform, das sogenannte „Eis-II“. Eis-II zeigt „normales Verhalten“, sein Schmelzpunkt steigt mit zunehmendem Druck.
Ergänzende Hinweise: Die Schmelzkurve beim Wasser unterscheidet sich von anderen Stoffen. Beim Schmelzen von Eis beobachtet man bei steigendem Druck ein Absinken des Schmelzpunktes. Dieses Phänomen nennt man Schmelzanomalie des Wassers. Das obige Zustandsdiagramm ist aus didaktischen und anschaulichen Gründen vereinfacht, außerdem sind im Diagramm die Proportionen nicht korrekt dargestellt. Bei sehr hohem Druck (nicht im Diagramm dargestellt) bildet das Eis eine weitere Zustandsform, das sogenannte „Eis-II“. Eis-II zeigt „normales Verhalten“, sein Schmelzpunkt steigt mit zunehmendem Druck.
Grenzen des Modells der
klassischen 3 Aggregatzustände
Nur einige Stoffe zeigen die klassischen Aggregatzustände mit den typischen Temperaturen bei den Umwandlungen. Manche Stoffe wie viele organische Stoffe zersetzen sich beim Erhitzen auch unter Luftabschluss. Es gibt Mineralien wie der Calcit, die sich gar nicht schmelzen lassen. Beim Quarz und bei vielen Gläsern ist der Übergang von fest nach flüssig fließend. Beim Erwärmen eines Glasröhrchens wird das Glas allmählich weich, beim weiteren Erhitzen zähflüssig, aber nie so flüssig wie das Wasser. Kristalliner Schwefel wird beim Erhitzen bei etwa 115 °C zunächst flüssig, dann tritt beim weiteren Erhitzen auf 159 °C eine zähflüssige Zustandsform auf, bevor er erneut flüssig wird und dann beim Siedepunkt ab 444 °C verdampft. All diese Phänomene lassen sich mit dem Modell der klassischen Aggregatzustände nicht mehr erklären.
Nur einige Stoffe zeigen die klassischen Aggregatzustände mit den typischen Temperaturen bei den Umwandlungen. Manche Stoffe wie viele organische Stoffe zersetzen sich beim Erhitzen auch unter Luftabschluss. Es gibt Mineralien wie der Calcit, die sich gar nicht schmelzen lassen. Beim Quarz und bei vielen Gläsern ist der Übergang von fest nach flüssig fließend. Beim Erwärmen eines Glasröhrchens wird das Glas allmählich weich, beim weiteren Erhitzen zähflüssig, aber nie so flüssig wie das Wasser. Kristalliner Schwefel wird beim Erhitzen bei etwa 115 °C zunächst flüssig, dann tritt beim weiteren Erhitzen auf 159 °C eine zähflüssige Zustandsform auf, bevor er erneut flüssig wird und dann beim Siedepunkt ab 444 °C verdampft. All diese Phänomene lassen sich mit dem Modell der klassischen Aggregatzustände nicht mehr erklären.
Kritik am oft verwendeten
Teilchenmodell
In einigen Schulbüchern wird das Teilchenmodell als „Erklärungsversuch“ für die klassischen Aggregatzustände hinzugezogen. Bei einem Feststoff sind die kleinsten Teilchen nach dieser Vorstellung nur wenig in Bewegung. Es wirken starke Anziehungskräfte, die Teilchen sind regelmäßig angeordnet und sie liegen relativ eng beieinander. Je höher die Temperatur ist, umso mehr nimmt die Eigenbewegung zu. Bei der Flüssigkeit ist die Bewegung der Teilchen so stark, dass die Teilchen nicht mehr ihren Platz halten können. Der Zusammenhalt der Teilchen ist jedoch weiter gewährleistet. Beim Gas sind die Teilchen so schnell in Bewegung, dass sie keine regelmäßige Anordnung mehr einnehmen können und auch nicht mehr zusammenhalten.
Kritik: Das Problem des Teilchenmodells ist, dass es mit Bildern aus der dem Menschen sichtbaren Welt arbeitet. Der Mikrokosmos ist aber eine abstrakte und andersartige Welt als die Welt, wie wir Menschen sie wahrnehmen und erkennen. Das Teilchenmodell legt den Schwerpunkt zu stark auf die bildhafte Darstellung der Teilchen, die als abgeschlossene Einheiten wie Pingpongbälle aufeinander „stoßen“ oder sich wie Magnete gegenseitig „anziehen“. Die komplizierten Wechselwirkungen der Systeme im atomaren Bereich werden nur unzureichend berücksichtigt.
Alternative: Die eingehende Beschäftigung mit den Phänomenen ist für ein einfaches Verstehen des Alltags aus didaktischer Sicht genügend präzise. Die komplizierteren Zusammenhänge werden durch die abstrakte Sprache der Mathematik treffend beschrieben, zum Beispiel durch eine Siedepunktkurve oder ein Zustandsdiagramm.
In einigen Schulbüchern wird das Teilchenmodell als „Erklärungsversuch“ für die klassischen Aggregatzustände hinzugezogen. Bei einem Feststoff sind die kleinsten Teilchen nach dieser Vorstellung nur wenig in Bewegung. Es wirken starke Anziehungskräfte, die Teilchen sind regelmäßig angeordnet und sie liegen relativ eng beieinander. Je höher die Temperatur ist, umso mehr nimmt die Eigenbewegung zu. Bei der Flüssigkeit ist die Bewegung der Teilchen so stark, dass die Teilchen nicht mehr ihren Platz halten können. Der Zusammenhalt der Teilchen ist jedoch weiter gewährleistet. Beim Gas sind die Teilchen so schnell in Bewegung, dass sie keine regelmäßige Anordnung mehr einnehmen können und auch nicht mehr zusammenhalten.
Kritik: Das Problem des Teilchenmodells ist, dass es mit Bildern aus der dem Menschen sichtbaren Welt arbeitet. Der Mikrokosmos ist aber eine abstrakte und andersartige Welt als die Welt, wie wir Menschen sie wahrnehmen und erkennen. Das Teilchenmodell legt den Schwerpunkt zu stark auf die bildhafte Darstellung der Teilchen, die als abgeschlossene Einheiten wie Pingpongbälle aufeinander „stoßen“ oder sich wie Magnete gegenseitig „anziehen“. Die komplizierten Wechselwirkungen der Systeme im atomaren Bereich werden nur unzureichend berücksichtigt.
Alternative: Die eingehende Beschäftigung mit den Phänomenen ist für ein einfaches Verstehen des Alltags aus didaktischer Sicht genügend präzise. Die komplizierteren Zusammenhänge werden durch die abstrakte Sprache der Mathematik treffend beschrieben, zum Beispiel durch eine Siedepunktkurve oder ein Zustandsdiagramm.
Weitere Aggregatzustände
Bei sehr hohen Temperaturen und sehr hohem Druck erreicht die Materie einen Zustand, der oft als vierter Aggregatzustand bezeichnet wird. Die Gase zerfallen dabei in ein Plasma, wobei die Elektronen der Atomhüllen in den Atomen ganz oder teilweise frei werden. Man erhält freie, negativ geladene Elektronen und positiv geladene Ionen. Materie im Plasmazustand besitzt völlig neue Eigenschaften. Sie ist in der Regel elektrisch sehr leitfähig und durch Magnetfelder leicht beeinflussbar. Plasmazustände finden sich oft in unserer Umwelt, ohne dass wir sie direkt wahrnehmen. So bilden Kerzenflammen oder Gewitterblitze teilweise Plasmazustände aus. Im Universum sind sie sehr häufig anzutreffen. Plasmen finden sich in den Sternen, beispielsweise im Inneren unserer Sonne. Neuerdings vermutet man auch sogenannte „metallische Plasmen“ im Inneren der Planeten, die dort unter hohem Druck und bei relativ niedriger Temperatur vorhanden sind. Im Labor kann man Plasmazustände durch starke Stromentladungen, durch die Verwendung von Laserstrahlen oder durch den Beschuss von Materie mit Schwerionenstrahlungen künstlich erzeugen.
Je mehr man bei einer Abkühlung der Materie dem absoluten Nullpunkt bei −273,15 °C nahe kommt, umso mehr verlieren die Atome ihre Individualität und funktionieren synchron. Eine Wechselwirkung zwischen den Atomen findet kaum noch statt. Ein Quantenphysiker spricht von einem einzigen Quantenzustand bei den Atomen. Dieser fünfte Aggregatzustand wird als Bose-Einstein-Kondensat oder BEC bezeichnet. Die Atome in einem solchen Zustand sind auch nicht mehr räumlich zuzuordnen. Man könnte auch sagen, die Atome sind im Kondensat überall zugleich. Vorausgesagt wurde dieser fünfte Aggregatzustand von Satyendra Nath Bose und Albert Einstein bereits im Jahre 1925. Der experimentelle Nachweis erfolgte im Jahre 1995 durch Eric Cornell, Carl Wiemann und Wolfgang Kettele, die im Jahr 2001 dafür den Nobelpreis erhielten.
Bei sehr hohen Temperaturen und sehr hohem Druck erreicht die Materie einen Zustand, der oft als vierter Aggregatzustand bezeichnet wird. Die Gase zerfallen dabei in ein Plasma, wobei die Elektronen der Atomhüllen in den Atomen ganz oder teilweise frei werden. Man erhält freie, negativ geladene Elektronen und positiv geladene Ionen. Materie im Plasmazustand besitzt völlig neue Eigenschaften. Sie ist in der Regel elektrisch sehr leitfähig und durch Magnetfelder leicht beeinflussbar. Plasmazustände finden sich oft in unserer Umwelt, ohne dass wir sie direkt wahrnehmen. So bilden Kerzenflammen oder Gewitterblitze teilweise Plasmazustände aus. Im Universum sind sie sehr häufig anzutreffen. Plasmen finden sich in den Sternen, beispielsweise im Inneren unserer Sonne. Neuerdings vermutet man auch sogenannte „metallische Plasmen“ im Inneren der Planeten, die dort unter hohem Druck und bei relativ niedriger Temperatur vorhanden sind. Im Labor kann man Plasmazustände durch starke Stromentladungen, durch die Verwendung von Laserstrahlen oder durch den Beschuss von Materie mit Schwerionenstrahlungen künstlich erzeugen.
Je mehr man bei einer Abkühlung der Materie dem absoluten Nullpunkt bei −273,15 °C nahe kommt, umso mehr verlieren die Atome ihre Individualität und funktionieren synchron. Eine Wechselwirkung zwischen den Atomen findet kaum noch statt. Ein Quantenphysiker spricht von einem einzigen Quantenzustand bei den Atomen. Dieser fünfte Aggregatzustand wird als Bose-Einstein-Kondensat oder BEC bezeichnet. Die Atome in einem solchen Zustand sind auch nicht mehr räumlich zuzuordnen. Man könnte auch sagen, die Atome sind im Kondensat überall zugleich. Vorausgesagt wurde dieser fünfte Aggregatzustand von Satyendra Nath Bose und Albert Einstein bereits im Jahre 1925. Der experimentelle Nachweis erfolgte im Jahre 1995 durch Eric Cornell, Carl Wiemann und Wolfgang Kettele, die im Jahr 2001 dafür den Nobelpreis erhielten.
Im Jahr 2003 stellte
ein Wissenschaftlerteam der Universität Colorado ein weiteres Kondensat
nahe dem absoluten Nullpunkt her. Das Kondensat aus Fermionen wurde gelegentlich
schon als sechster Aggregatzustand bezeichnet. Ob das Fermionen-Kondensat einen
sechsten Aggregatzustand oder nur eine Variante des fünften darstellt,
ist noch nicht endgültig geklärt.
Ob ein Vakuum als Aggregatzustand bezeichnet werden kann, ist umstritten. Ein Vakuum ist entstanden, wenn die diversen Phänomene, die aus einem Gas bekannt sind, nicht mehr auftreten:
Ob ein Vakuum als Aggregatzustand bezeichnet werden kann, ist umstritten. Ein Vakuum ist entstanden, wenn die diversen Phänomene, die aus einem Gas bekannt sind, nicht mehr auftreten:
- Es treten keine Strömungsphänomene wie Verwirbelungen oder Sog mehr auf.
- Die Schallleitung ist vollständig unterbrochen.
- Ein Luftwiderstand tritt nicht mehr auf.
- Wärme wird nur durch Wärmestrahlung übertragen.
Powerpointpräsentationen
Digitale Folien
Buch individuell erstellen: Basis-Text Aggregatzustände


> Inhaltsverzeichnis