|
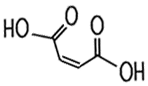 Weißes, kristallines Pulver oder prismatische Kristalle |
Molmasse 116,073 g/mol AGW keine Angaben Dichte 1,590 g/cm3 Zersetzung +139 °C Wasserlöslichkeit Konz. bei 20 °C 789 g/l Flammpunkt +127 °C Zündpunkt keine Angaben |
| Piktogramme GHS 07 Achtung |
Gefahrenklassen
+ Kategorie Akute Toxizität oral 4 Ätz-/Reizwirkung auf die Haut 2 Augenreizung 2 Spez. Zielorgantoxizität e. 3 (Atemwege) Hautsensibilisierung 1 |
HP-Sätze (siehe auch Hinweis) H 302, 315, 317, 319, 335 P 261, 280.1-3, 302+352, 305+351+338 Entsorgung G 3 |
| Etikett drucken | Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
| CAS 110-16-7 |
Maleinsäure cis-Butendisäure |
Maleic acid cis-Butenedioic acid |
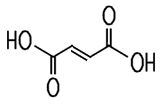
| Eigenschaften Die Maleinsäure ist im Handel als weißes, kristallines Pulver erhältlich. Zur Fumarsäure besteht eine cis-trans-Isomerie. Während im Molekül der Furmarsäure die trans-Konfiguration vorliegt, findet sich im Maleinsäure-Molekül die cis-Konfiguration.
Dies führt zu erheblichen Unterschieden bei den chemisch-physikalischen Eigenschaften. Die Maleinsäure ist viel besser wasserlöslich und sie ist weniger stabil. Sie unterscheidet sich auch in der Dichte zur Furmarsäure. In der Natur kommt die Maleinsäure nicht vor. Sie wird vom menschlichen Körper auch weniger gut akzeptiert. So kann sie zum Beispiel allergische Reaktionen auf der Haut auslösen. Maleinsäure und ihre Salze, die Maleate, haben ein nierenschädigendes Potenzial.  Beim Erwärmen isomerisiert Maleinsäure zur Fumarsäure. Beim Erhitzen auf über 150 °C bildet sie unter Wasserabspaltung Maleinsäureanhydrid, das zu farblosen Nadeln kristallisiert. Dieses reagiert mit Wasser wieder unter Bildung der Maleinsäure. Maleinsäure löst sich auch gut in Ethylalkohol und etwas weniger gut in Aceton und Diethylether. |
| Herstellung Maleinsäure wird durch die Reaktion von Maleinsäureanhydrid mit Wasser gewonnen. Das Anhydrid gewinnt man durch die Oxidation von Benzol an der Luft bei 450°C und dem Vorliegen eines Vanadiumpentoxid-Katalysators. Dabei spaltet sich das Benzol-Molekül auf, und Sauerstoff-Atome bauen sich in das Molekül ein. Eine andere Herstellungsmöglichkeit ist die Oxidation von Buten, das beim Cracken anfällt. 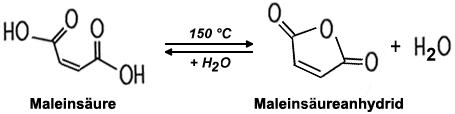 |
| Verwendung Maleinsäure
und Maleinsäureanhydrid werden zur Herstellung von
Maleinsäureestern, Kunststoffen und Kunstharzen benötigt. Mit
Maleinsäure vorbehandelte Baumwolle lässt sich mit basischen
Farbstoffen besser färben. |