 Teflonverschluss |
Weißes, kristallines Pulver Vorkommen Harz des Kampferbaums, etherische Öle in Pflanzen |
Molmasse 152,233 g/mol AGW keine Angaben Dichte 0,990 g/cm3 Schmelzpunkt +178,7 °C Siedepunkt +209 °C Wasserlöslichkeit Konz. bei 20 °C 0,1 g/l Explosionsgrz. 0,6 bis 3,5 Vol.-% (Luft) Flammpunkt +66 °C Zündpunkt +466 °C |
| Piktogramme GHS 02 GHS 07 Gefahr |
Gefahrenklassen
+ Kategorie Entzündbare Feststoffe 1 Reizwirkung auf die Haut 2 Augenreizung 2 Spez. Zielorgan-Tox. e. Atemwege 3 |
HP-Sätze (siehe auch Hinweis) H 228, 315, 319, 335 P 210, 280.1–3, 302+352, 304+340, 305+351+338 Entsorgung G 3 |
| Etikett drucken | Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
| CAS 76-22-2 (unspezifisch) |
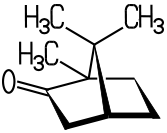
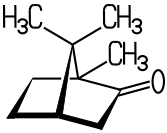
Campher 1,7,7-Trimethylbicyclo(2.2.1)heptan-2-on 2-Bornanon |
Camphor 1,7,7-Trimethylbicyclo(2.2.1)heptan-2-one 2-Bornanone |
| Wirkung auf den menschlichen Körper Campher wirkt als
Analeptikum anregend auf das Nervensystem und auf die Atmungsorgane,
sofern er in geringen Dosen eingesetzt wird. Er erzeugt auf der Haut ein
Wärmegefühl und eine leichte Rötung, da die Durchblutung
gefördert wird. Beim Einatmen der Dämpfe findet
allmählich ein Gewöhnungseffekt statt, so dass der Geruch
nicht mehr wahrgenommen wird. Die orale Aufnahme führt zu einem
leichten Brennen auf den Schleimhäuten. Bei höheren
Dosierungen können Kopfschmerzen, Erbrechen, Schwindel,
Halluzinationen oder Zittern auftreten. Schwere Vergiftungen
äußern sich in Krämpfen oder in einer Atemlähmung,
die sogar tödlich verlaufen kann. Es können auch Nieren- oder
Leberschädigungen auftreten. Zwei Gramm innerlich eingenommen
lösen schon schwere Vergiftungserscheinungen aus.
Eigenschaften Campher
bildet weiße, orthorhombische Kristalle oder ein kristallines
Pulver mit einem eukalyptusartigen, herb-aromatischen Geruch.
Campher schmeckt scharf und bitter. Er ist in Wasser und Glycerin kaum
löslich, in Alkohol und anderen organischen Lösungsmitteln wie
Diethylether, Aceton oder fetten Ölen löst er sich gut.
Campher sublimiert bereits bei Zimmertemperatur. Er ist gut brennbar und
verbrennt mit rußender Flamme. An der Luft ist Campher relativ
beständig, er oxidiert auch nicht beim Erhitzen.  In der Natur kommen zwei Enantiomere mit Spiegelbild-Isomerie vor. In der Rinde und im Harz des Kampferbaumes findet man aber überwiegend den rechtsdrehenden (+)-Campher. Im Chemikalienhandel erhält man meistens ein unspezifiziertes Racemat der beiden Enantiomere. Es sind aber auch die reinen Formen erhältlich.
|
| Herstellung Campher
kann durch Wasserdampfdestillation aus der geraspelten Rinde und dem
Harz der Kampferbaumes gewonnen werden. Durch Umkristallisation wird das
Rohprodukt gereinigt. Synthetisch kann man Campher in mehreren
Zwischenschritten aus α-Pinen herstellen, das in zahlreichen etherischen Ölen vorkommt, beispielsweise im Terpentinöl.
|
| Verwendung Campher wird als
Duftstoff in Kosmetika verwendet. In Verbindung mit Baumharzen findet er
sich in Räucherstäbchen. Salben mit bis zu zehn Prozent
Campher dienen als Mittel gegen Rheuma, Muskelzerrungen oder
entzündlichen Ödemen. In Erkältungssalben wirken die
Dämpfe zusammen mit anderen Stoffen wie Eukalyptusöl zur
Inhalation entzündungshemmend auf die Bronchialschleimhaut. Das in
Apotheken erhältliche Kampferöl zur Bekämpfung von
Erkältungskrankheiten ist eine 10%ige Campher-Lösung in
Erdnussöl.
Die chemische Industrie benötigt Campher zur Herstellung von Celluloid und als Weichmacher für Celluloseester. In Feuerwerkskörpern wird Campher als Brennstoff eingesetzt, dort erzeugt er zusammen mit Schwefel und einem Oxidationsmittel eine funkensprühende Verbrennung. Campher wird auch bei der Herstellung von Sprenggelatine benötigt. In Mottenkugeln vertreibt er die kleiderfressenden Insekten. Im Chemieunterricht kann man mit Campher aufgrund des niedrigen Tripelpunktes (179 °C bei 493 mbar) die Sublimation und die Resublimation bei vermindertem Druck im geschlossenen System in einer Vakuum-Sublimationsapparatur demonstrieren. Dazu wird wenig Campher in das Gefäß mit Seitenrohr gegeben. Am Seitenrohr wird eine Vakuumpumpe angeschlossen. In der Apparatur sitzt ein mit Wasser gekühlter Kühlfinger. Daran resublimiert dann der Campher. Die Sublimation und Resublimation kann auch im offenen System bei Normaldruck durch einfaches Erhitzen gezeigt werden: In einem größeren Reagenzglas wird wenig Campher erhitzt. Im darin stehenden kleineren Reagenzglas befindet sich Eis zur Kühlung oder man verwendet einen Kühlfinger. Das resublimierte Produkt ist reiner als das Ausgangsprodukt. Auf diese Art und Weise kann man rohen Campher reinigen. |