Schritt 1: Ammoniak + Sauerstoff![]() Stickstoffmonooxid + Wasser ΔHR
= −908 kJ/mol
Stickstoffmonooxid + Wasser ΔHR
= −908 kJ/mol
4 NH3
+ 5 O2 ![]() 4 NO + 6 H2O
4 NO + 6 H2O
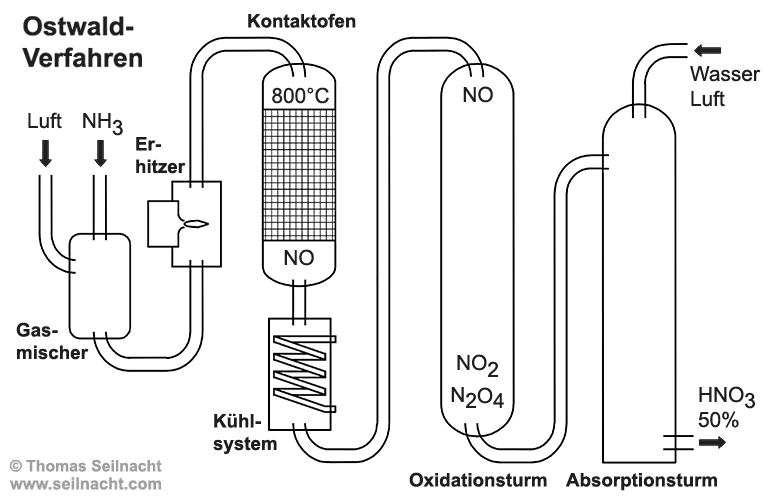
In einem nachgeschalteten Kühlsystem wird danach das Stickstoffmonooxid unter 50 °C gekühlt und in den Oxidationsturm geleitet. Dort oxidiert das Stickstoffmonooxid mit Sauerstoff zu Stickstoffdioxid. Diese Reaktion ist erst bei Temperaturen unterhalb 50 °C durchführbar. Unter den vorherrschenden Bedingungen entsteht in einer Gleichgewichtsreaktion auch Distickstofftetraoxid.
Schritt 2: Stickstoffmonooxid + Sauerstoff ![]() Stickstoffdioxid ΔHR
= −114 kJ/mol
Stickstoffdioxid ΔHR
= −114 kJ/mol
2 NO
+ O2 ![]() 2 NO2
2 NO2
Stickstoffdioxid![]() Distickstofftetraoxid ΔHR
= −57 kJ/mol
Distickstofftetraoxid ΔHR
= −57 kJ/mol
2 NO2 ![]() N2O4
N2O4
In den nachfolgenden Absorptionstürmen wird das Stickstoffoxid-Gemisch mit herabrieselndem Wasser unter Luftzugabe zu einer 50%igen Salpetersäure umgesetzt, die durch eine nachgeschaltete Destillationsanlage auf etwa 65 % konzentriert werden kann. Das dabei anfallende Stickstoffmonooxid wird wieder in den Oxidationsturm zurückgeleitet und nach Schritt 2 erneut oxidiert. Mögliche Nebenreaktionen sind hier nicht dargestellt. Eine moderne Anlage kann täglich bis zu 1200 Tonnen Salpetersäure herstellen.
Schritt 3: Stickstoffdioxid + Wasser ![]() Salpetersäure + Stickstoffmonooxid
Salpetersäure + Stickstoffmonooxid
3 NO2 + H2O ![]() 2 HNO3 + NO
2 HNO3 + NO
Distickstofftetraoxid + Sauerstoff + Wasser ![]() Salpetersäure
Salpetersäure
2 N2O4 + O2 + 2 H2O ![]() 4 HNO3
4 HNO3
Zum Ostwald-Verfahren liegt eine Serie in 9 Bildern zur Lösungskontrolle vor. Die Lösungen werden beim Durchklicken im Vollbildmodus nach und nach eingeblendet. Die Serie kann zur Erarbeitung des Arbeitsblattes verwendet werden. Es liegt auch ein Text vor, den man gleichzeitig vorlesen kann.

 Serie starten
Serie startenArbeitsblatt doc docx pdf
Vorlesetext doc docx pdf
Buch individuell erstellen: Basis-Text Salpetersäure


> Inhaltsverzeichnis