Natürliche Stoffe aus der Gruppe der Alkanthiole wirken toxisch auf das Zentralnervensystem und zeichnen sich durch einen besonders widerwärtigen Geruch aus. Sie kommen als Aromastoffe in Milch, Käse, Zwiebeln und Knoblauch
vor. Beim Abbau und bei Fäulnisprozessen von organischem Material
werden Alkanthiole gebildet. Sie entstehen auch beim Erhitzen von
Eiweiß. Das Drüsensekret des Stinktiers enthält als
Hauptbestandteil 2-Butenthiol (40%). Weitere übelriechende
Alkanthiole wie 3-Methylbutanthiol (22%), 2-Chinolinmethanthiol (8%)
und andere Stoffe kommen im Stinktier-Sekret ebenfalls vor.
Alkanthiole werden auch Thioalkohole genannt, da bei ihnen das Sauerstoff-Atom der Alkohole durch ein Schwefel-Atom ersetzt ist. Die SH-Gruppe nennt man Mercapto- oder Thiol-Gruppe. In der chemischen Industrie bezeichnet man die Alkanthiole als Mercaptane. Methanthiol oder Methylmercaptan ist der einfachste Vertreter. Kurzkettige Alkanthiole stellen eine Geruchskomponente des Erdöls dar.
Alkanthiole werden auch Thioalkohole genannt, da bei ihnen das Sauerstoff-Atom der Alkohole durch ein Schwefel-Atom ersetzt ist. Die SH-Gruppe nennt man Mercapto- oder Thiol-Gruppe. In der chemischen Industrie bezeichnet man die Alkanthiole als Mercaptane. Methanthiol oder Methylmercaptan ist der einfachste Vertreter. Kurzkettige Alkanthiole stellen eine Geruchskomponente des Erdöls dar.
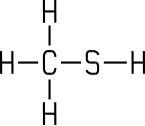
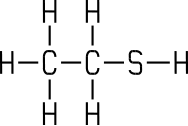
| Methanthiol | Ethanthiol | Propanthiol |
|
 |
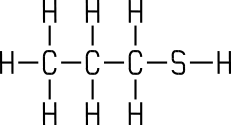 |
| Sdp. 6°C | Sdp. 35°C | Sdp. 68°C |
Methanthiol (Methylmercaptan)
Methylmercaptan ist ein sehr übelriechendes,
giftiges und brennbares Gas, das die Augen und die Atemwege reizt. Der
faulige und stechende Geruch ist selbst in geringsten Konzentrationen wahrnehmbar,
daher treten Vergiftungen relativ selten auf. Es entsteht bei der bakteriellen
Zersetzung von Eiweiß und verursacht den Geruch von gekochtem Kohl.
In Wasser ist es nicht löslich, dafür in Ethanol und Diethylether.
Es dient als Ausgangsstoff zur Herstellung von Aminosäuren, Pflanzenschutzmitteln
und Kunststoffen. Die technische Herstellung des Methylmercaptans erfolgt
aus Methanol und Schwefelwasserstoff
bei etwa 400 °C und einem wolframaktiven Aluminiumoxid-Katalysator:
CH3OH + H2S
Methanol + Schwefelwasserstoff
Ethanthiol (Ethylmercaptan)
Ethylmercaptan ist eine übelriechende,
giftige Flüssigkeit, die ebenfalls in geringsten Konzentrationen noch
wahrnehmbar ist. Die Geruchsschwelle liegt bei einem Milligramm pro Tonne. Es kommt im Steinkohleteer und im Erdöl
vor. Wie Methanthiol ist es ein wichtiges Zwischenprodukt für organische
Synthesen. Es wird zusammen mit Propanthiol als Warngas im Erdgas zum
Aufspüren von Lecks und Rohrbrüchen verwendet.
Eigenschaften der Alkanthiole
Die Siedetemperaturen der Alkanthiole sind niedriger als die der Alkohole, da sich im Molekül keine Wasserstoffbrücken ausbilden können. Ihre Säurestärke ist im Vergleich zu den Alkoholen höher, daher bilden sie mit Natriumhydroxid gerne Salze, die als Thiolate bezeichnet werden:
Eigenschaften der Alkanthiole
Die Siedetemperaturen der Alkanthiole sind niedriger als die der Alkohole, da sich im Molekül keine Wasserstoffbrücken ausbilden können. Ihre Säurestärke ist im Vergleich zu den Alkoholen höher, daher bilden sie mit Natriumhydroxid gerne Salze, die als Thiolate bezeichnet werden:
CH3SH + NaOH
Methanthiol + Natriumhydroxid
Bei der Oxidation mit Wasserstoffperoxid erhält man Disulfide wie
Dimethyldisulfid CH3-S-S-CH3, mit starken
Oxidationsmitteln wie Salpetersäure oder Kaliumpermanganat entstehen
Sulfonsäuren, beispielsweise Methansulfonsäure CH3SO3H. Diese dient als Ausgangsstoff zur Herstellung von Waschmitteln.
Buch individuell erstellen: Basis-Text Thioalkohole


> Inhaltsverzeichnis
Buch individuell erstellen: Basis-Text Thioalkohole


> Inhaltsverzeichnis
