 |
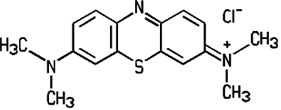 Kupferrote Kristalle, olivgrünes Pulver |
Molmasse 319,852 g/mol AGW keine Angaben Dichte 1,0 g/cm3 Schmelzpunkt 190 °C (Zersetzung) Wasserlöslichkeit Konz. bei 20°C 40g/l |
| Piktogramme GHS 07 Achtung |
Gefahrenklassen
+ Kategorie Akute Toxizität oral 4 |
HP-Sätze (siehe auch Hinweis) H 302 P 264.1, 280.1-3, 301+312 Entsorgung G 3 |
| Etikett drucken | Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
| CAS 61-73-4 | Methylenblau Methylthioniniumchlorid Blue Basic 9 C.I. 52015 |
Methylene Blue Methylthioninium chloride Blue Basic 9 C.I. 52015 |
Besondere Bemerkungen: Da Farbstoffe stark färben und auch Haut, Augen und Atemwege reizen, sind Schutzbrille und Schutzhandschuhe zu tragen, beim Freiwerden von Stäuben muss eine Feinstaubmaske aufgezogen oder im Abzug gearbeitet werden.
Eigenschaften Methylenblau bildet
kupferrote Kristalle, die in fein zerteilter Form oder bei Kontakt mit
Luftsauerstoff olivgrün schimmern. Der Feststoff ist gut brennbar.
Mit Luft können Stäube explosionsgefährliche Mischungen
bilden. Mit Wasser bildet Methylenblau eine intensive, cobaltblaue
Lösung, die sauer reagiert. Schon geringste Mengen erzeugen eine
Blaufärbung. Methylenblau ist auch in Ethanol leicht löslich.
 Der basische
Thiazinfarbstoff färbt mit Tannin vorgebeizte Baumwolle blau.
Lebendes Zellmaterial wie Zellwände oder Zellkerne, aber auch
Bakterien, Fasern und sogar Papier werden durch Methylenblau direkt
gefärbt. Die Färbung erfolgt selektiv, so lässt sich die
graue Substanz im peripheren Nervensystem anfärben. Diese Methode
wandte der deutsche Arzt Paul Ehrlich im Jahr 1885 erstmals an. Die
Molekularbiologie verwendet Methylenblau zum Färben von DNA und
RNA.  |
| Herstellung Die technische Herstellung des Farbstoffes erfolgt durch die Oxidation von p-Aminodimethylanilin, Dimethylanilin und Natriumthiosulfat mit Chromsäure unter Zugabe von Zinkchlorid und Salzsäure. |
| Verwendung Methylenblau ist in
der Mikroskopie ein weit verbreiteter Vital-Farbstoff zum Anfärben
von lebendem Material. Löfflers Methylenblaulösung ist eine
0,5%ige Lösung in Wasser, die zum Färben von Bakterien, Pilzen
und Blutparasiten eingesetzt wird. May-Grünwald-Lösung ist
eine methanolische Lösung von Methylenblau und Eosin. Früher
wurde Methylenblau in blauer Tinte verwendet,
heute kommt stattdessen meistens ein blauer
Triphenylmethanfarbstoff zum Einsatz. In der Medizin wird Methylenblau
als Gegengift bei Nitrit- und Anilinvergiftungen eingesetzt: Es wandelt
im Blut das bei der Vergiftung gebildete Methämoglobin wieder zum
lebenswichtigen Hämoglobin um, das den Sauerstofftransport
gewährleistet. Methylenblau dient auch als Wunddesinfektionsmittel
(Antiseptikum), zur Bekämpfung der Malaria, sowie in Medikamenten
gegen Rheuma. Kläranlagen stellen mit der Methylenblauprobe fest,
wie viel Fäulnisstoffe im Ablauf der Kläranlage enthalten sind:
Methylenblau wird unter Luftabschluss durch Fäulnisstoffe
reduziert und verliert dabei seine Farbe. 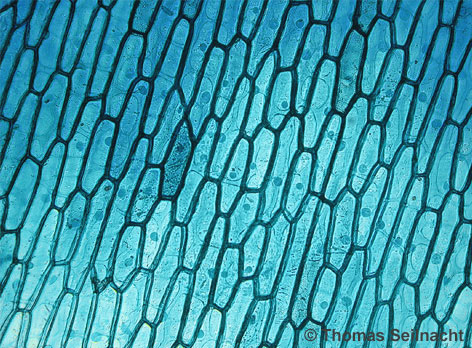 Zwiebelzellen, angefärbt mit Methylenblau |