Elemente und Verbindungen
Experimente mit Kupferacetat

|
Stoffe |
Kupfer(II)-acetat,
Kupfer Blech ca. 10 × 5 cm, Essigessenz (Essigsäure 25%) |
|
Geräte |
Schutzbrille, Brenner und Streichhölzer, Reagenzglas, RG-Halter, Glaswolle, Schraubglas |
|
|
Schutzbrille tragen und Schutzhandschuhe anziehen! Stoffe nicht anfassen! Beim Erhitzen Kopf fernhalten! Nicht direkt am Reagenzglas riechen! Nur bei aktiver Raumlüftung durchführen! Nach dem Experimentieren Hände waschen! Reaktionsprodukte ordnungsgemäß entsorgen! |
| GBU Deutschland | Erhitzen von Kupfer(II)-acetat docx pdf |
| SB Schweiz | Erhitzen von Kupfer(II)-acetat docx pdf |
Dieser Versuch stellt
eine harmlosere Variante der früher an den Schulen angewandten Zersetzung
des stark toxischen Quecksilberoxids dar.
Erhitzt man eine Spatelspitze Kupfer(II)-acetat
in einem hitzebeständigen Reagenzglas mit der nicht leuchtenden Brennerflamme, verfärbt
es sich bräunlich und ein gelber Rauch steigt auf. Dabei riecht es
stark nach Essig. An der Wand des Reagenzglases entsteht ein schöner
Kupferspiegel. Führt man den Versuch als Schülerübung durch, wird das Reagenzglas mit wenig Glaswolle locker verschlossen, so dass noch Gas entweichen kann, aber das Kupfer im Reagenzglas zurückbleibt.
Die Beobachtungen weisen
darauf hin, dass Kupferacetat in Kupfer
und Essigsäure zerlegt wird.
Die chemische Verbindung Kupfer(II)-acetat ist ein Stoff, der (in einer
endothermen Reaktion) in mindestens zwei weitere Stoffe „zerlegt“ werden
kann. Das Kupfer selbst kann nicht mehr weiter zerlegt werden, es ist ein
chemisches Element. Doch diese Definition
soll den Schülerinnen und Schülern zunächst vorenthalten werden.
Initiation
Der beschriebene Versuch
wird vorgeführt oder die Schülerinnen und Schüler führen ihn selbst durch.
In einem gemeinsamen Gespräch sollen sie sich überlegen, ob sie
schon eine Vermutung für das beobachtete Phänomen finden. Diese könnte zum Beispiel so formuliert werden:
- Stoff a (Kupferacetat) wird zerlegt in zwei weitere Stoffe;
- Kupferacetat enthält Atomverbände zwischen Kupfer-Atomen und „Essigsäure“ (falls das Vorwissen aus dem Versuch „Kupfer + Schwefel“ noch vorhanden ist), diese werden getrennt.
|
|
Dies sollen die Lernenden jedoch selbst herausfinden. Der Inhalt des Behälters wird nach Beendigung des Experiments im Behälter für Schwermetallsalze entsorgt. Die Schülerinnen und Schüler erhalten diese Arbeitsaufträge:
1.) Führe das Experiment durch und erstelle einen ausführlichen Bericht!
2.) Suche im Internet oder in Büchern nach diesen Begriffen: Kupferacetat, Grünspan, chemisches Element, chemische Verbindung! Sammle auch Informationen über mögliche Gefahren!
3.) Versuche die Beobachtungen aus deinem Experiment mit Hilfe der nachgeschlagenen Begriffe zu erklären!
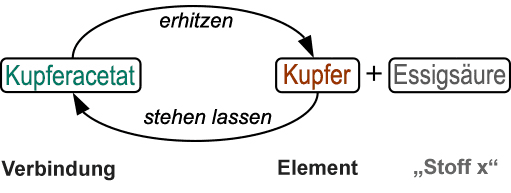
Die Berichte werden besprochen und diskutiert. Es kann dann auch gezeigt
werden, dass der Versuch umkehrbar ist, in dem man die gebildeten Kristalle
wieder erhitzt. Das Schema unten dient zur Erläuterung.
Dabei genügt der
Hinweis, dass „Stoff x“ ebenfalls eine chemische Verbindung darstellt,
die mit geeigneten Mitteln noch weiter zerlegt werden könnte.
Entsorgung:
Reste des Kupferacetats werden im Behälter für feste,
organische Abfälle entsorgt. Nach der Entsorgung des Kupferacetats
werden die Reagenzgläser gut gewaschen und gespült. Geht der
Kupferspiegel nicht weg, gibt man die Reagenzgläser zum
Glasmüll. Generell wird empfohlen, den Glasmüll vom
Restmüll zu trennen (Verletzungsgefahr!) und jeweils einen Metallbehälter mit Deckel zu verwenden.