Ein
Reagenzglas wird zur Hälfte mit verdünnter Salzsäure der Konzentration 1 Mol pro Liter gefüllt. Bei der Zugabe von Zink-Stückchen
entsteht in einer lebhaften Reaktion Wasserstoff,
den man pneumatisch in einem Messzylinder auffängt. Für die Reaktion
wird folgende Reaktionsgleichung angegeben:
2 HCl + Zn
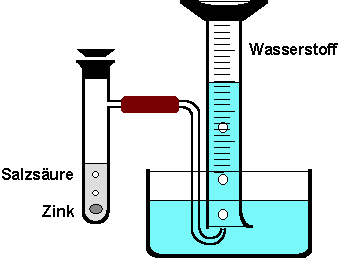
Im ersten Experiment
wird das Volumen genau nach einer Minute abgelesen, die Zink-Stückchen
entnommen und die Konzentration der verbleibenden Säure bestimmt.
Im zweiten Experiment verfährt man genau gleich und führt die
Messungen nach zwei Minuten durch, usw. Die Ergebnisse werden in einer Tabelle
eingetragen:
| Experiment | Start | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Zeit (Minuten) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Konzentration HCl (Mol pro Liter) | 1 | 0,8 | 0,6 | 0,42 | 0,28 | 0,18 | 0,11 | 0,07 | 0,04 | 0,02 | 0 |
| Gasvolumen H2 (Milliliter) | 0 | 10 | 20 | 30 | 40 | 47 | 50 | 52 | 53 | 54 | 55 |
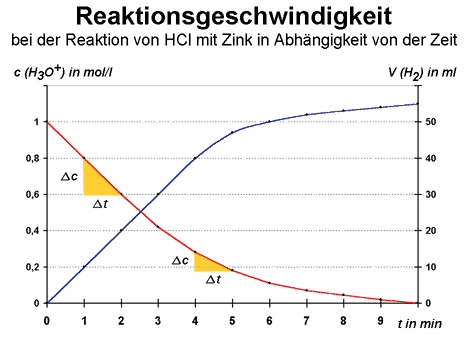
Das Ablaufen dieser chemischen
Reaktion hängt von der Reaktionsgeschwindigkeit v ab. Darunter versteht
man die Änderung der Konzentration an Ausgangs-Stoffen (oder an Produkten)
pro Zeitspanne, in der diese Änderung eintritt:
v = Δc ÷ Δt
Beim ersten Experiment nahm die Konzentration der Salzsäure in einer Minute um 0,2 Mol pro Liter ab.
Somit ergibt sich für den Ausgangs-Stoff (HCl) diese Reaktionsgeschwindigkeit:
v = 0,2 mol/l ÷ 60 s = 0,0333 mol/l s
Misst man weitere Zeitintervalle, stellt man fest, dass die Reaktionsgeschwindigkeit allmählich abnimmt. Dies hängt mit der Abnahme der Konzentration der Salzsäure zusammen, am Ende der Reaktion bildet sich auch immer weniger Wasserstoff pro Zeiteinheit. Als Beispiel wird die Reaktionsgeschwindigkeit zwischen dem Zeit-Intervall nach vier bis fünf Minuten bestimmt:
v = 0,1 mol/l ÷ 60 s = 0,0166 mol/l s
Die Reaktionsgeschwindigkeit ist nun nur noch halb so groß. Dies wird auch auf der folgenden Grafik verdeutlicht. Die Abnahme der Reaktionsgeschwindigkeit kann an der abnehmenden Steilheit der absteigenden Kurve abgelesen werden:
v = 0,2 mol/l ÷ 60 s = 0,0333 mol/l s
Misst man weitere Zeitintervalle, stellt man fest, dass die Reaktionsgeschwindigkeit allmählich abnimmt. Dies hängt mit der Abnahme der Konzentration der Salzsäure zusammen, am Ende der Reaktion bildet sich auch immer weniger Wasserstoff pro Zeiteinheit. Als Beispiel wird die Reaktionsgeschwindigkeit zwischen dem Zeit-Intervall nach vier bis fünf Minuten bestimmt:
v = 0,1 mol/l ÷ 60 s = 0,0166 mol/l s
Die Reaktionsgeschwindigkeit ist nun nur noch halb so groß. Dies wird auch auf der folgenden Grafik verdeutlicht. Die Abnahme der Reaktionsgeschwindigkeit kann an der abnehmenden Steilheit der absteigenden Kurve abgelesen werden:
Führt man das obige
Experiment mit konzentrierter Salzsäure durch, dann entsteht
mehr Wasserstoff in einer kürzeren Zeit-Einheit. Die Konzentration
der Salzsäure nimmt schneller ab, die Reaktionsgeschwindigkeit erhöht
sich. Eine Beschleunigung wird auch durch eine Temperatur-Erhöhung erreicht.
Dabei gilt die Faustregel: Bei einer Erhöhung der Temperatur um 10
Kelvin (10 °C) steigt die Reaktionsgeschwindigkeit mindestens um das
Doppelte. Verwendet man statt Zinkstücken pulverförmiges Zink,
ist ebenfalls eine erhöhte Gasentwicklung sichtbar. Dies lässt
sich experimentell jedoch nur mit frisch reduziertem Zink zeigen. Je
größer die Oberfläche und je größer der Zerteilungsgrad
der reagierenden Stoffe ist, desto größer ist die Reaktionsgeschwindigkeit.
Bestimmte Faktoren begünstigen also die Reaktionsgeschwindigkeit:
-
Erhöhung der Konzentration der reagierenden Stoffe
-
Temperaturerhöhung
-
Feinere Zerteilung und Erhöhung der wirksamen Oberfläche
Eine Erhöhung der Konzentration bedeutet, dass mehr reagierende Systeme pro Volumen vorhanden sind. Die Erhöhung des Zerteilungsgrades vergrößert die wirksame Oberfläche, dadurch können mehr Ereignisse pro Zeiteinheit stattfinden. Diese Faktoren wirken kinetisch.
Welche Rolle spielen die Aktivierungsenergie und ein Katalysator?
Die Differenz der Energieniveaus zwischen Ausgangsstoffen (Edukten) und Endstoffen (Produkten) wird bei einer chemischen Reaktion als freie Enthalpie ΔGR bezeichnet. Sie gibt an, ob eine Reaktion von selbst ablaufen kann (exergonische Reaktion ΔG<0) oder ob die kontinuierliche Zufuhr von Energie notwendig ist (endergonische Reaktion ΔG>0). Chemische Reaktionen verlaufen jedoch nicht direkt von den Ausgangsstoffen zu den Endstoffen. Auf dem Reaktionsweg wird ein kurzzeitig instabiler Übergangszustand durchlaufen. Das Erreichen dieses Zustands ist besonders energieaufwändig.
Als Aktivierungsenergie wird derjenige Energiebetrag bezeichnet, der notwendig ist, um die Reaktion einzuleiten. Eine Wärmezufuhr begünstigt also das Ablaufen der Reaktion.
Ein Katalysator verändert den Reaktionsweg so, dass der Übergangszustand leichter erreichbar ist. Dadurch verläuft die Reaktion schneller, ohne die freie Enthalpie der Reaktion zu verändern.
Welche Rolle spielen die Aktivierungsenergie und ein Katalysator?
Die Differenz der Energieniveaus zwischen Ausgangsstoffen (Edukten) und Endstoffen (Produkten) wird bei einer chemischen Reaktion als freie Enthalpie ΔGR bezeichnet. Sie gibt an, ob eine Reaktion von selbst ablaufen kann (exergonische Reaktion ΔG<0) oder ob die kontinuierliche Zufuhr von Energie notwendig ist (endergonische Reaktion ΔG>0). Chemische Reaktionen verlaufen jedoch nicht direkt von den Ausgangsstoffen zu den Endstoffen. Auf dem Reaktionsweg wird ein kurzzeitig instabiler Übergangszustand durchlaufen. Das Erreichen dieses Zustands ist besonders energieaufwändig.
Als Aktivierungsenergie wird derjenige Energiebetrag bezeichnet, der notwendig ist, um die Reaktion einzuleiten. Eine Wärmezufuhr begünstigt also das Ablaufen der Reaktion.
Ein Katalysator verändert den Reaktionsweg so, dass der Übergangszustand leichter erreichbar ist. Dadurch verläuft die Reaktion schneller, ohne die freie Enthalpie der Reaktion zu verändern.
Buch individuell erstellen: Basis-Text Reaktionsgeschwindigkeit


> Inhaltsverzeichnis