|
Lebenslauf
Svante Arrhenius wurde am 19. Februar 1859 als Sohn des Akademievogts der Universität Uppsala geboren. Bereits im Alter von 3 Jahre lernte er lesen. Dadurch, dass er dem Vater bei seiner Arbeit an den Rechnungsbüchern zuschaute, prägte sich bei dem jungen Svante ein Sinn für Zahlenreihen ein. In der Domschule zu Uppsala fiel er besonders durch seine Begabung in Mathematik und Physik auf. Nach dem Abitur begann der 17-Jährige Svante sein Studium an der Universität in Uppsala in den Fächern Mathematik und Naturwissenschaften. Mit dem Physikunterricht an dieser Universität war Arrhenius unzufrieden, daher wechselte er 1881 zur Universität nach Stockholm. 1884 erschien seine Doktorarbeit "Recherches sur la conductibilité galvanique des électrolytes" in französischer Sprache. In dieser Arbeit legte der junge Arrhenius seine revolutionären Theorien über die Dissoziation von Salzen dar. Die Arbeit stieß zunächst bei vielen Chemikern auf Ablehnung, sie veranlasste aber, dass der deutsch-baltische Chemiker (und spätere Nobelpreisträger) Wilhelm Ostwald die Arbeit las und Arrhenius' Theorien unterstützte. Ostwald bot ihm daraufhin sogar einer Stelle in Riga an. Die beiden Chemiker unternahmen eine gemeinsame Reise nach Magdeburg. Aufgrund der prominenten Unterstützung erhielt Arrhenius 1884 eine Anstellung an der Universität in Uppsala. Mit Hilfe eines Reisestipendiums der Schwedischen Akademie der Wissenschaften konnte Arrhenius ab 1886 an verschiedenen Orten in Europa mit namhaften Wissenschaftlern zusammenarbeiten: 1886 bei Wilhelm Ostwald in Riga und bei Friedrich Wilhelm Georg Kohlrausch (1840-1910) in Würzburg, 1887 bei Ludwig Boltzmann (1844-1906) in Graz und 1888 bei Jacobus Hendricus van t'Hoff (1852-1911) in Amsterdam. Die Reisen endeten mit einem erneuten Aufenthalt bei Ostwald, der unterdessen in Leipzig eine Professur erhalten hatte. Ab 1891 erhielt Arrhenius eine feste Anstellung an der Universität Stockholm, wo er dann 1895 Professor für Physik wurde. 1903 folgte der Nobelpreis für Chemie für seine Arbeiten über die elektrolytische Dissoziation. Ab 1905 übernahm Arrhenius die Direktion des Nobelinstituts für physikalische Chemie. Obwohl die Ämter für ihn viel Arbeit und Pflichten mit sich brachten, erschienen zahlreiche Publikationen, beispielsweise" Theorien der Chemie" (1906), "Immunochemie" (1907), "Theories of Solutions" (1918) oder "Erde und Weltall" (1926). Arrhenius vertrat in dem Buch "Das Werden der Welten" (1906), die Ansicht, dass das Leben durch Meteorite auf die Erde gelangt ist (Panspermie-Lehre). Dieses eher populärwissenschaftlich geschriebene Werk knüpfte an sein Buch "Lehrbuch der kosmischen Physik" (1903) an. Svante Arrhenius starb nach kurzer Krankheit am 2. Oktober 1927 an einem Darmkatarrh. Theorien und Werk Arrhenius' Theorien über die Dissoziation von Salzen in Lösungen legten den Grundstein für die moderne Säure-Base-Theorie nach Johannes Nicolaus Brönsted (1879-1947), die in jedem Schulbuch heute dargestellt ist. Vor Arrhenius war man der Ansicht, dass Ionen nur durch das Anlegen einer elektrischen Spannung, beispielsweise bei der Elektrolyse einer Salzlösung, entstehen konnten. Dass das Kochsalz auch beim bloßen Lösen in Wasser schon Ionen bildet, war eine der grundlegenden Theorien seiner Doktorarbeit aus dem Jahr 1884. Wilhem Ostwald äußerte sich später so dazu: "Mir ist noch die Szene im chemischen Laboratorium zu Uppsala vor Augen, wo der Chef, selbst ein hochbedeutender Chemiker, mich entsetzt fragte, indem er auf ein Becherglas mit einer wässrigen Lösung hinzeigte: 'Und Sie glauben auch, dass dort die Natriumatome nur so herumschwimmen?'..." (aus W. Palmaer in G. Bugge: Das Buch der großen Chemiker, S. 451) In der Doktorarbeit von 1884 werden zunächst Experimente beschrieben, in denen Arrhenius mit stark verdünnten Salzlösungen arbeitete und ihre Leitfähigkeit bestimmte. Die daraus abgeleiteten Theorien stellt er dann in der Form von 56 Thesen vor. In der ersten These wird beispielsweise behauptet, dass die elektrische Leitfähigkeit für stark verdünnte Lösungen proportional zur Konzentration ist. Arrhenius nahm auch an, dass die Salze in Lösungen nur zu einem bestimmten Anteil dissoziiert, also in Ionen zerfallen sind. Wilhelm Ostwalds führte dafür den Begriff des Dissoziationsgrades ein, der angibt, wie groß der Anteil an gelösten Ionen in einer Elektrolytlösung ist. Petrus Debye (1884-1966) und Erich Hückel (1896-1980) wiesen im Jahr 1923 die Unzulänglichkeit der Arrhenius-Ostwaldschen Theorie nach. Nach der Debye-Hückel-Theorie sind starke Elektrolyte vollständig, also zu 100% dissoziiert. Durch Arrhenius konnten Säuren und Basen neu definiert werden: Wässrige Säuren enthalten in ihrer Lösung positiv geladene Wasserstoff-Ionen und negativ geladene Säurerest-Ionen, Basen dagegen positiv geladene Baserest-Ionen und Hydroxid-Ionen. Von Bedeutung sind auch seine Arbeiten zur Reaktionsgeschwindigkeit. Durch Experimente fand er empirisch einen Zusammenhang zwischen der Temperatur und der Geschwindigkeit einer chemischen Reaktion. Die Abhängigkeit beschrieb Arrhenius mit seiner Arrheniusgleichung: 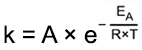 k, Reaktionsgeschwindigkeitskonstante A, Arrheniuskonstante EA, Aktivierungsenergie R, Gaskonstante (8,314 J pro K × mol) T, absolute Temperatur Die Arrheniusgleichung ist nicht mehr genau, wenn man chemische Reaktionen in einem großen Temperaturbereich untersucht, da sich dann die Arrheniuskonstante ändert. Gelegentlich wird die Gleichung auch in ihrer logarithmischen Form dargestellt: 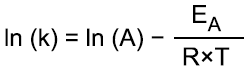 Bestimmt man k bei mindestens drei verschiedenen Temperaturen, dann lässt sich die Aktivierungsenergie EA einer chemischen Reaktion bestimmen. Svante Arrhenius war ein vielseitiger Wissenschaftler, der Zusammenhänge sah. Seine Publikationen zur Geophysik und Kosmologie sollen hier nicht näher erläutert werden. Interessant dazu ist vielleicht seine erstmals aufgestellte Behauptung, dass das Kohlenstoffdioxid an der Erwärmung der Erdatmosphäre beteiligt ist (siehe >Treibhauseffekt). Empfehlenswerte Literaturquellen
|